Staatscourant van het Koninkrijk der Nederlanden
| Datum publicatie | Organisatie | Jaargang en nummer | Rubriek |
|---|---|---|---|
| Ministerie van Volksgezondheid, Welzijn en Sport | Staatscourant 2006, 220 pagina 32 | Besluiten van algemene strekking |
Zoals vergunningen, bouwplannen en lokale regelgeving.
Adressen en contactpersonen van overheidsorganisaties.
U bent hier:

| Datum publicatie | Organisatie | Jaargang en nummer | Rubriek |
|---|---|---|---|
| Ministerie van Volksgezondheid, Welzijn en Sport | Staatscourant 2006, 220 pagina 32 | Besluiten van algemene strekking |
Regeling van de Minister van Volksgezondheid, Welzijn en Sport van 7 november 2006, nr. VGP/VV 2726743, houdende wijziging van de Warenwetregeling Gebruik van additieven met uitzondering van kleurstoffen en zoetstoffen in levensmiddelen en van de Warenwetregeling Gebruik van zoetstoffen in levensmiddelen
De Minister van Volksgezondheid, Welzijn en Sport,
Gelet op richtlijn nr. 2006/52/EG van het Europees Parlement en de Raad van de Europese Unie van 5 juli 2006 (PbEU L 204) tot wijziging van richtlijn 95/2/EG betreffende levensmiddelenadditieven met uitzondering van kleurstoffen en zoetstoffen, en richtlijn 94/35/EG inzake zoetstoffen die in levensmiddelen mogen worden gebruikt, alsmede op artikel 7, tweede lid, van het Warenwetbesluit Levensmiddelenadditieven;
Besluit:
De Warenwetregeling Gebruik van additieven met uitzondering van kleurstoffen en zoetstoffen in levensmiddelen1 wordt als volgt gewijzigd:
A
Artikel 1, eerste lid, onder f, komt te luiden:
f. draagstoffen: stoffen, met inbegrip van de oplosmiddelen die als draagstoffen fungeren, die gebruikt worden om een additief op te lossen, te verdunnen, te dispergeren of op een andere wijze fysisch te wijzigen zonder de technologische functie daarvan te veranderen (en zonder zelf enig technologisch effect uit te oefenen), teneinde de verwerking, de toepassing of het gebruik van het additief te vergemakkelijken;.
B
Bijlage I wordt als volgt gewijzigd:
1. Direct vóór de tabel met opsomming van E-nummers wordt ingevoegd:
De stoffen E 400, E 401, E 402, E 403, E 404, E 406, E 407, E 407a, E 410, E 412, E 413, E 414, E 415, E 417, E 418 en E 440 worden niet gebruikt in geleiproducten met een vaste consistentie in halfstijve minicups of minicapsules die bedoeld zijn om in één hap te worden gegeten door in de minicup of minicapsule te knijpen waardoor de waar in de mond komt.
2. In de opsomming van E-nummers met naam wordt ingevoegd na E 461 Methylcellulose:
E 462 Ethylcellulose.
C
Bijlage II wordt als volgt gewijzigd:
1. Bij het levensmiddel ‘Gerijpte kaas’ wordt aan de kolommen Additief en Maximumconcentratie toegevoegd:

2. In de kolom Levensmiddel worden aan ‘PAIN COURANT FRANÇAIS’ op een nieuwe regel de volgende woorden toegevoegd: FRISS BÚZAKENYÉR, FEHÉR ÉS FÉLBARNA KENYEREK.
3. In de kolom Levensmiddel worden aan ‘FOIE GRAS, FOIE GRAS ENTIER, BLOCS DE FOIE GRAS’ op een nieuwe regel de volgende woorden toegevoegd: LIBAMÀJ, LIBAMÀJ EGÉSZBEN, LIBAMÀJ TÖMBBEN.
D
Bijlage III wordt als volgt gewijzigd:
1. In deel I. Conserveermiddelen, onder A. Sorbaten, benzoaten en p-hydroxy-benzoaten, tweede alinea, vervalt: E216 (propyl-p-hydroxybenzoaat), E217 (propyl-p-hydroxybenzoaat, natriumzout),.
2. In de tabel in deel I, onder A, worden de volgende levensmiddelen met bijbehorende maximumconcentratie geschrapt:

3. De volgende levensmiddelen met bijbehorende maximumconcentraties worden toegevoegd aan de tabel in deel I, onder A:

4. In de tabel in deel I, onder A, wordt in de kolom Levensmiddelen ‘Dieetvoeding voor medisch gebruik met uitzondering van voeding voor zuigelingen, opvolgzuigelingenvoeding en babyvoeding als bedoeld in het Warenwetbesluit Produkten voor bijzondere voeding’ vervangen door: Dieetvoeding voor medisch gebruik, bedoeld in de Warenwetregeling Dieetvoeding voor medisch gebruik, met uitzondering van volledige zuigelingenvoeding en opvolgzuigelingenvoeding, bedoeld in de Warenwetregeling Zuigelingenvoeding, en van babyvoeding, bedoeld in de Warenwetregeling Babyvoeding.
5. In de tabel in deel I, onder B, wordt het Levensmiddel ‘Schaaldieren en cefalopoden’ met bijbehorende maximumconcentraties vervangen door:
Schaaldieren en koppotigen | ||
– | vers, bevroren en diepgevroren | 1501 |
– | schaaldieren, familie van de Penaiedae, Solenoceridae, Aristaeidae: | |
– tot 80 eenheden | 1501 | |
– van 80 tot en met 120 eenheden | 2001 | |
– meer dan 120 eenheden | 3001 | |
Schaaldieren en koppotigen: | ||
– | gekookt | 501 |
– | gekookte schaaldieren, familie van de Penaiedae, Solenoceridae, Aristaeidae: | |
– tot 80 eenheden | 1351 | |
– van 80 tot en met 120 eenheden | 1801 | |
– meer dan 120 eenheden | 2701 | |
1 In eetbare delen.
6. In de tabel in deel I, onder B, wordt in de kolom Levensmiddel ‘Zetmeel, met uitzondering van zetmeel voor zuigelingenvoeding, opvolgzuigelingenvoeding en babyvoeding, zoals omschreven in het Warenwetbesluit Produkten voor bijzondere voeding’ vervangen door: Zetmeel, met uitzondering van volledige zuigelingenvoeding en opvolgzuigelingenvoeding, bedoeld in de Warenwetregeling Zuigelingenvoeding, en van bewerkte eet- of drinkwaren op basis van granen, en babyvoeding, bedoeld in de Warenwetregeling Babyvoeding.
7. Aan de tabel in deel I, onder B, wordt toegevoegd:
SALSICHA FRESCA | 450 |
Tafeldruiven | 10 |
Verse lychees | 101 |
1 Gemeten in eetbare delen
8. In de tabel in deel I, onder C. Andere Conserveermiddelen, worden de E-nummers E 249, E 250, E 251 en E 252, met bijbehorende vermeldingen, vervangen door:
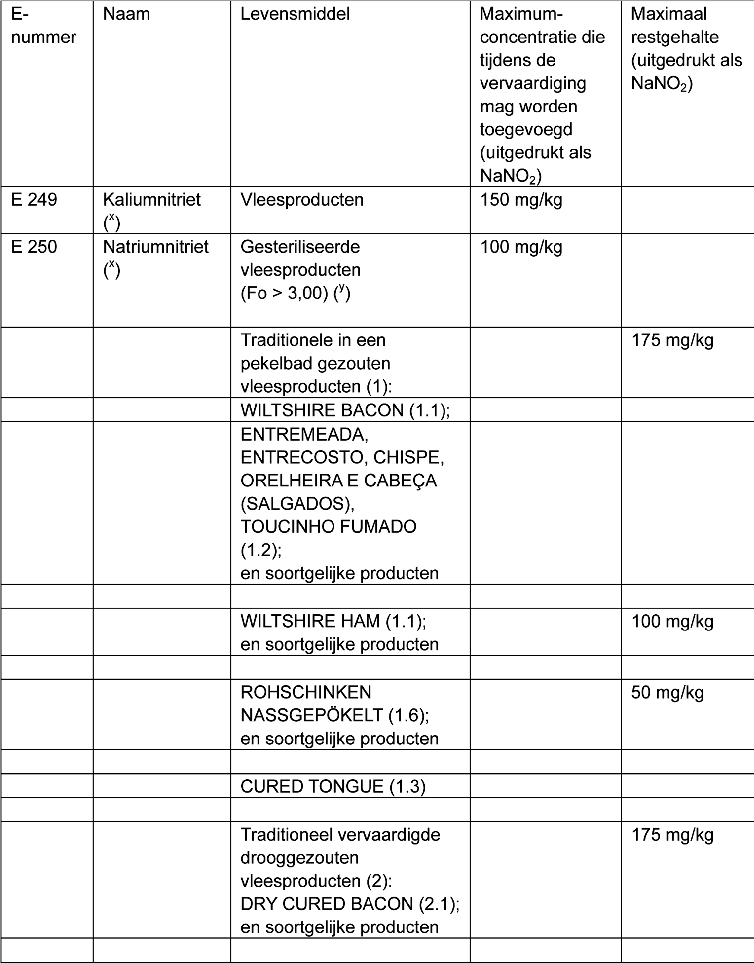
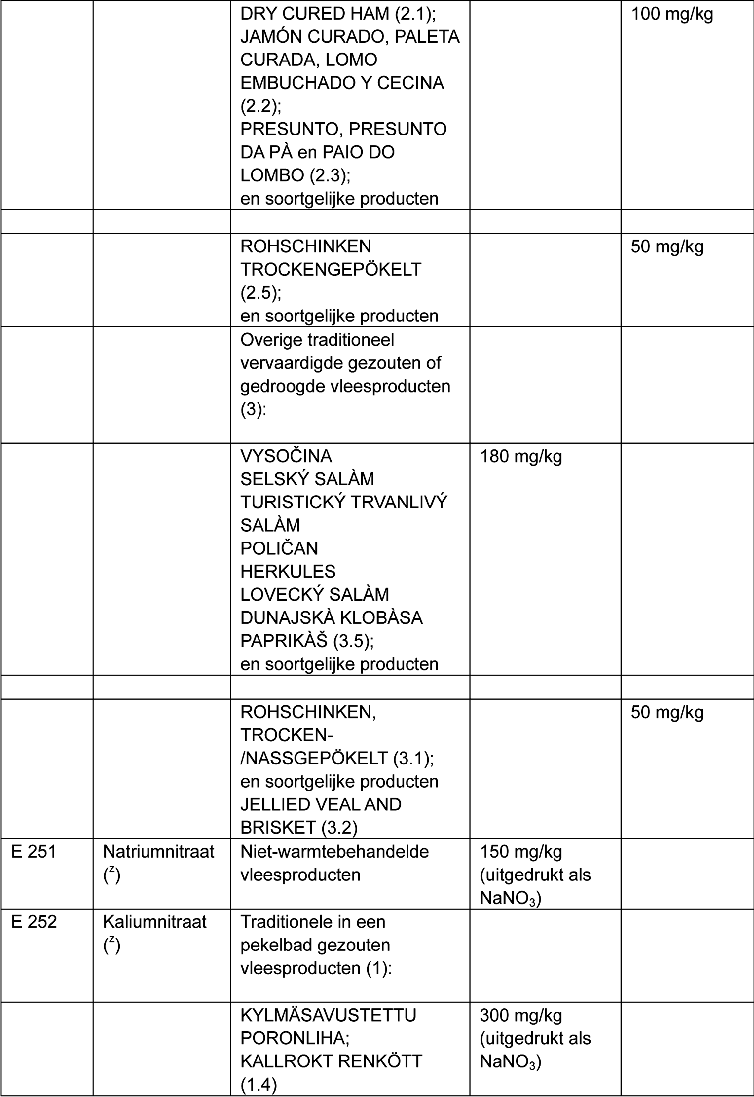
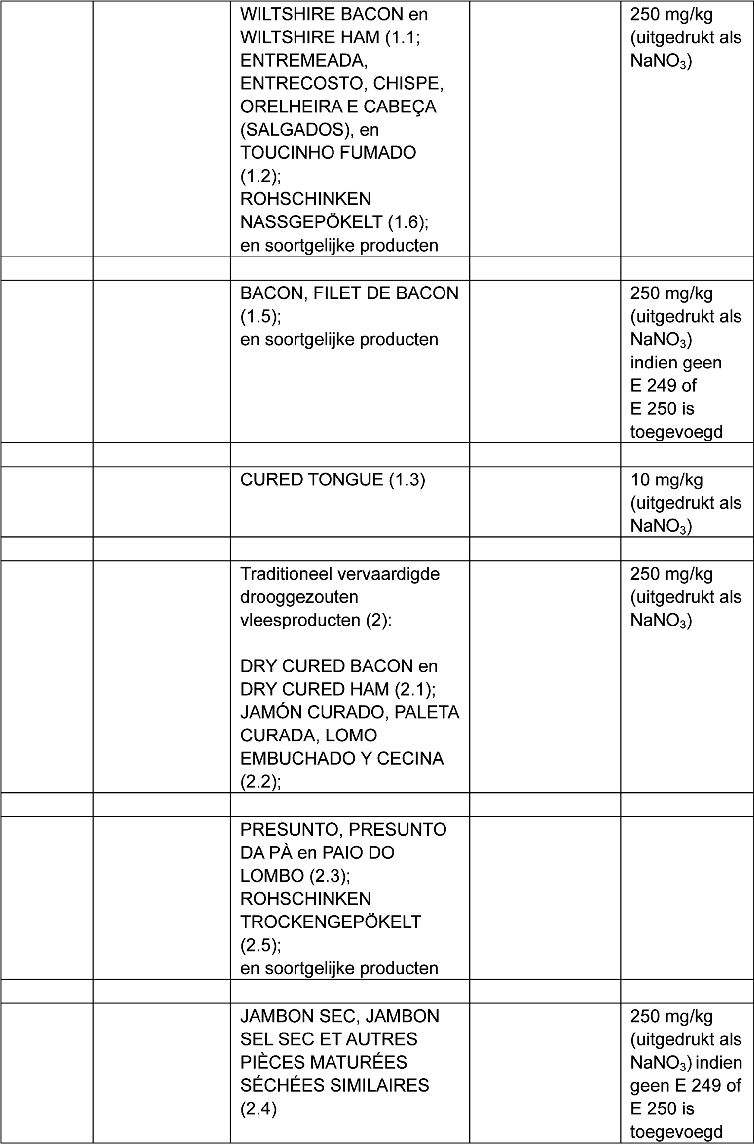
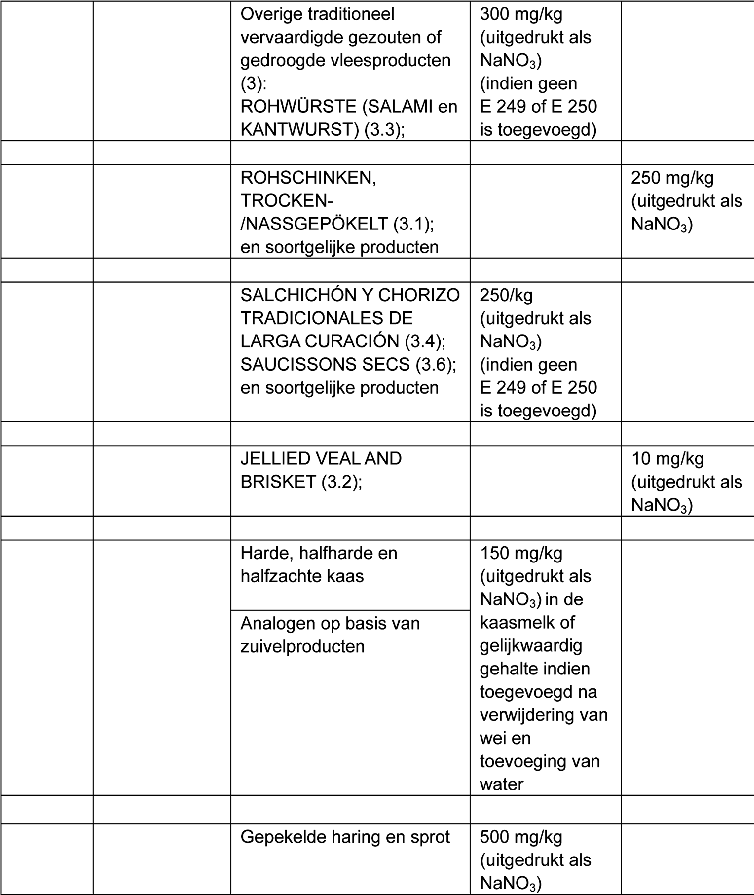
(x) Nitriet met de vermelding ‘voor gebruik in voeding’ mag alleen vermengd met zout of met een zoutvervanger verkocht worden.
(y) Een Fo-waarde 3 staat gelijk met verhitting gedurende drie minuten bij 121 °C (vermindering van de bacteriële verontreiniging van een miljard sporen per 1000 blikken tot één spore per 1000 blikken).
(z) In sommige warmtebehandelde vleesproducten kunnen nitraten aanwezig zijn die voortkomen uit de natuurlijke omzetting van nitrieten in nitraten in een zuurarme omgeving.
1 De vleesproducten worden in een pekeloplossing van nitrieten of nitraten, zout en andere bestanddelen gedompeld. Deze vleesproducten kunnen verdere behandelingen ondergaan, bijvoorbeeld worden gerookt.
1.1 Het vlees wordt ingespoten met een pekeloplossing en vervolgens gedurende drie à tien dagen in een pekelbad gezouten. De bij onderdompeling gebruikte pekeloplossing omvat microbiologische startculturen.
1.2 Zouten in een pekelbad gedurende drie à vijf dagen. Product heeft geen hittebehandeling ondergaan en heeft een hoge wateractiviteit.
1.3 In een pekelbad gezouten gedurende ten minste vier dagen en voorgekookt.
1.4 Het vlees wordt ingespoten met een pekeloplossing, gevolgd door zouten in een pekelbad. De pekeltijd bedraagt 14 à 21 dagen, daarna rijping (koudroken) gedurende vier à vijf weken.
1.5 Het vlees wordt in een pekelbad gezouten gedurende vier à vijf dagen bij 5–7 °C, waarna het rijpt gedurende normaliter 24 à 40 uur bij 22 °C, eventueel wordt het gerookt gedurende 24 à 40 uur bij 22 °C, eventueel wordt het gerookt gedurende 24 uur bij 20–25 °C en wordt bewaard gedurende drie à zes weken bij 12–14 °C.
1.6 De pekeltijd is, afhankelijk van de vorm en het gewicht van de vleesstukken, ongeveer 2 dagen/kg gevolgd door stabilisatie/rijping.
2. Bij droogzouten wordt de buitenkant van het vlees (droog) ingewreven met een pekelmengsel dat nitrieten of nitraten, zout en andere bestanddelen bevat, gevolgd door stabilisatie/rijping. Deze vleesproducten kunnen verdere behandelingen ondergaan, bijvoorbeeld worden gerookt.
2.1 Droogzouten gevolgd door rijping gedurende ten minste vier dagen.
2.2 Droogzouten met een stabilisatieperiode van ten minste tien dagen en een rijpingsperiode van ten minste 45 dagen.
2.3 Droogzouten gedurende 10 à 15 dagen, gevolgd door een stabilisatieperiode van 30 à 45 dagen en een rijpingsperiode van ten minste twee maanden.
2.4 Droogzouten gedurende drie dagen + één dag/kg, gevolgd door een week bewaring na het zouten en een verouderings-/rijpingsperiode van 45 dagen tot 18 maanden.
2.5 De pekeltijd, afhankelijk van de vorm en het gewicht van de vleesstukken, is ongeveer 10 tot 14 dagen/kg gevolgd door stabilisatie/rijping.
3 Combinatie van zouten in een pekelbad en droogzouten, of waarbij nitrieten of nitraten bestanddeel zijn van een samengesteld product of waarbij de pekeloplossing in het product wordt ingespoten voordat het wordt gekookt. Deze producten kunnen verdere behandelingen ondergaan, bijvoorbeeld worden gerookt.
3.1 Combinatie van droogzouten en zouten in een pekelbad (zonder inspuiten van pekeloplossing). De rooktijd afhankelijk van de vorm en het gewicht van de vleesstukken, is ongeveer 14 tot 35 dagen/kg gevolgd door stabilisatie/rijping.
3.2 Het vlees wordt ingespoten met een pekeloplossing en vervolgens, na ten minste twee dagen, gekookt in kokend water gedurende ten hoogste 3 uur.
3.3 Het product is gedurende ten minste vier weken gerijpt met een water/proteïne-verhouding van minder dan 1,7.
3.4 Rijping gedurende ten minste 30 dagen.
3.5 Het gedroogde product wordt gekookt bij 70 °C, waarna het gedurende acht à twaalf dagen wordt gedroogd en gerookt. Gefermenteerd product, onderworpen aan een fermentatieproces van 14 à 30 dagen in drie fasen, waarna het wordt gerookt.
3.6 Gedroogde gefermenteerde rauwe worst zonder toevoeging van nitrieten. Het product wordt gefermenteerd bij een temperatuur van 18–22 °C of lager (10–12 °C) en ondergaat vervolgens gedurende ten minste drie weken een verouderings-/rijpingsproces. Het product heeft een water/proteïne-verhouding van minder dan 1,7.
9. Deel II. Antioxydanten wordt als volgt gewijzigd:
a. De eerste alinea vóór de tabel komt te luiden:
Het teken * in de tabel wijst op de evenredigheidsregel: als combinaties van gallaten, TBHQ, BHA en BHT worden gebruikt, worden de afzonderlijke gehaltes evenredig verminderd.
b. In de tabel worden de E-nummers E 310, E 311, E 312, E 320 en E 321, met bijbehorende vermeldingen, vervangen door:
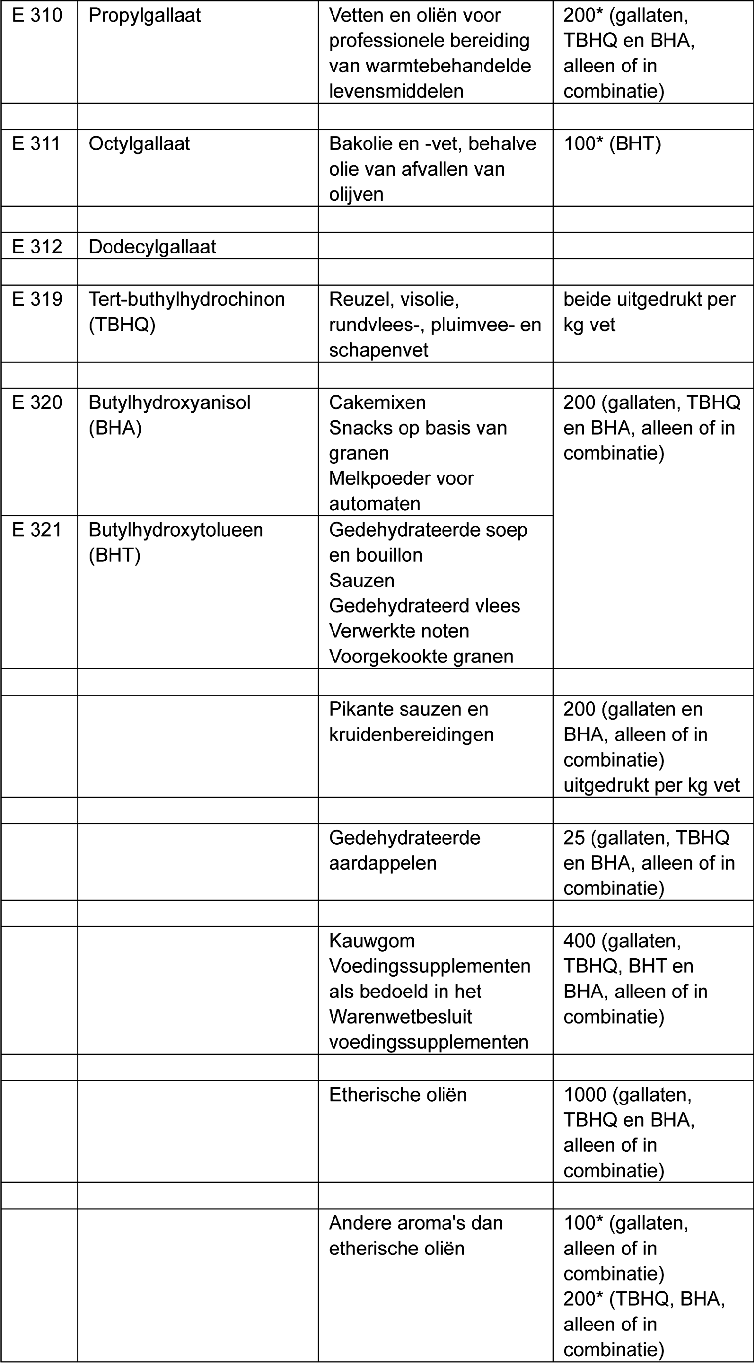
c. Toegevoegd wordt:

10. Deel III. Andere additieven wordt als volgt gewijzigd:
a. E-nummer 385 met bijbehorende vermeldingen wordt vervangen door:

b. Na E-nummer 967 met bijbehorende vermeldingen wordt ingevoegd:

c. Het volgende E-nummer met bijbehorende vermeldingen wordt toegevoegd:
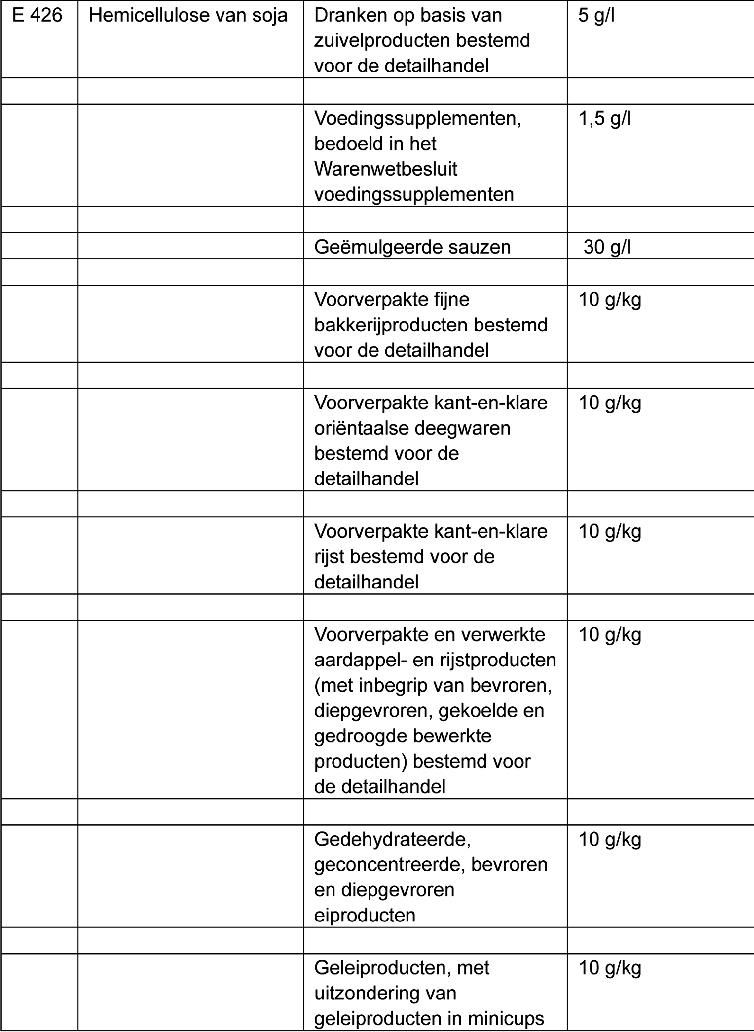
d. Bij de volgende E-nummers wordt ‘Voedingssupplementen’ steeds vervangen door: ‘Voedingssupplementen, bedoeld in het Warenwetbesluit voedingssupplementen’:
1°. E 338 tot en met E 452;
2°. E 405;
3°. E 416;
4°. E 432 tot en met E 436;
5°. E 468;
6°. E 473 en E 474;
7°. E 475;
8°. E 491 tot en met E 495;
9°. E 551 tot en met E 559;
10°. E 901 tot en met E 904.
e. Bij de volgende E-nummers wordt ‘Dieetvoedsel voor speciale medische doeleinden’ steeds vervangen door: ‘Dieetvoeding voor medisch gebruik, bedoeld in de Warenwetregeling Dieetvoeding voor medisch gebruik’:
1°. E 405;
2°. E 432 tot en met E 436;
3°. E 473;
4°. E 474;
5°. E 475;
6°. E 477;
7°. E 481;
8°. E 482;
9°. E 491 tot en met E 495.
f. Bij de E-nummers E 1201 en E 1202 wordt ‘Voedingssupplementen in tablet- of drageevorm’ vervangen door: Voedingssupplementen, bedoeld in het Warenwetbesluit voedingssupplementen, in tablet- of drageevorm.
g. De E-nummers E 1505 tot en met E 1520 met bijbehorende vermeldingen worden vervangen door:
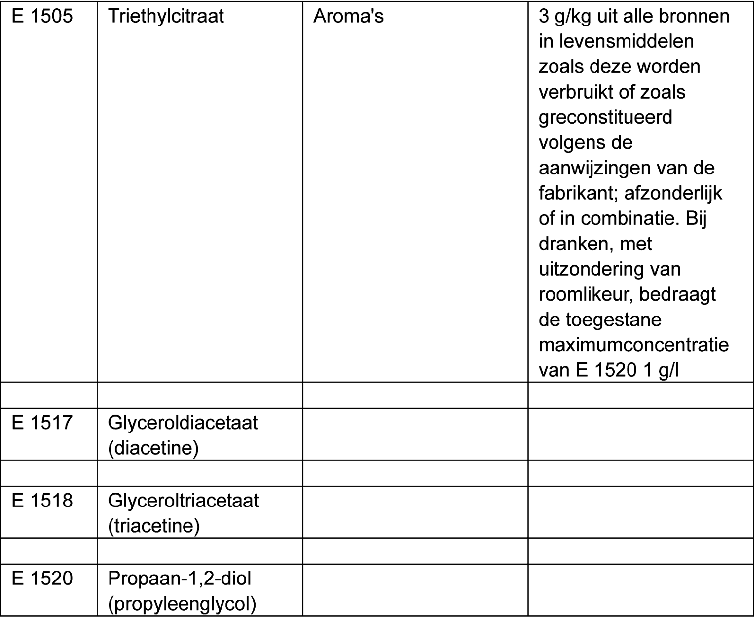
h. De volgende E-nummers met bijbehorende vermeldingen worden toegevoegd:
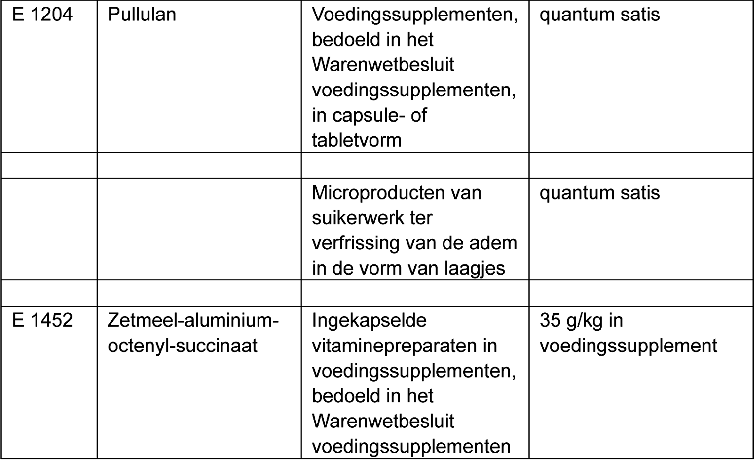
E
Bijlage IV wordt als volgt gewijzigd:
1. Aan de E-nummers E 420 tot en met E 967 wordt toegevoegd:

2. Bij de E-nummers E 460 tot en met E 466 wordt na E 461 ingevoegd:

3. Aan de kolom ‘Beperkt gebruik’ wordt bij de E-nummers E 551 en E 552 een zin toegevoegd, luidende:
Voor E 551: in E 171 Titaandioxide en E 172 IJzeroxiden en -hydroxiden (maximaal 90% in verhouding tot het pigment).
F
Bijlage V wordt als volgt gewijzigd:
1. In de tekst vóór deel I wordt ‘bijvoedingsmiddelen’ steeds vervangen door: bewerkte eet- of drinkwaren op basis van granen en babyvoeding.
2. De titel ‘Deel. III ADDITIEVEN DIE ZIJN TOEGELATEN IN BABYVOEDING’ wordt vervangen door: Deel III. ADDITIEVEN DIE ZIJN TOEGELATEN IN BEWERKTE EET- OF DRINKWAREN OP BASIS VAN GRANEN EN BABYVOEDING.
3. In deel III wordt bij de volgende E-nummers ‘bijvoedingsmiddelen’ steeds vervangen door: bewerkte eet- of drinkwaren op basis van granen en babyvoeding:
a. E 170 tot en met E 526;
b. E 500 tot en met E 503;
c. E 338;
d. E 410 tot en met E 440;
e. E 1404 tot en met E 1451.
4. Aan deel IV wordt toegevoegd:

De bijlage van de Warenwetregeling Gebruik van zoetstoffen in levensmiddelen wordt als volgt gewijzigd:
1. In de eerste kolom wordt aan de E-nummers E 420 tot en met E 967 toegevoegd: E 968.
2. In de tweede kolom wordt achter E 968 vermeld: Erytritol.
Eet- en drinkwaren die vóór 15 augustus 2008 in de handel zijn gebracht en die voldoen aan:
a. de Warenwetregeling Gebruik van additieven met uitzondering van kleurstoffen en zoetstoffen in levensmiddelen; en
b. de Warenwetregeling Gebruik van zoetstoffen in levensmiddelen;
zoals die luidden onmiddellijk vóór de inwerkingtreding van artikel I onderscheidenlijk artikel II van deze regeling, mogen worden verhandeld zolang de voorraad strekt.
1. Deze regeling treedt in werking met ingang van de tweede dag na de dagtekening van de Staatscourant waarin zij wordt geplaatst.
2. In afwijking van het eerste lid treedt artikel II in werking met ingang van 1 februari 2007.
Deze regeling zal met de toelichting in de Staatscourant worden geplaatst.
Op 26 juli 2006 is gepubliceerd richtlijn nr. 2006/52/EG van het Europees Parlement en de Raad van de Europese Unie van 5 juli 2006 (PbEU L 204) tot wijziging van richtlijn 95/2/EG betreffende levensmiddelenadditieven met uitzondering van kleurstoffen en zoetstoffen, en richtlijn 94/35/EG inzake zoetstoffen die in levensmiddelen mogen worden gebruikt, verder te noemen: richtlijn 2006/52/EG.
Richtlijn 2006/52/EG brengt bepaalde regels voor levensmiddelenadditieven in overeenstemming met de laatste technische ontwikkelingen. Ter uitvoering daarvan dienen twee Warenwetregelingen te worden aangepast:
a. de Warenwetregeling Gebruik van additieven met uitzondering van kleurstoffen en zoetstoffen in levensmiddelen;
b. de Warenwetregeling Gebruik van zoetstoffen in levensmiddelen.
Deze regeling zorgt daarvoor.
Bij deze wijzigingsregeling zijn met name bijlagen van deze twee Warenwetregelingen gewijzigd. Indien daarbij een eet- of drinkwaar in hoofdletters is vermeld, betekent dit – zo blijkt uit de desbetreffende te wijzigen bijlagen – dat uitsluitend de als zodanig aangeduide waar de desbetreffende additieven mag bevatten.
Bij deze implementatie is een kennelijke fout in richtlijn 2006/52/EG hersteld. De maximumconcentratie en het maximale restgehalte van E 251 en E 252, bedoeld in artikel I, onder D, punt 8, zijn uitgedrukt als NaNO3 (en niet als NaNO2 zoals abusievelijk is vermeld in de richtlijn).
De overwegingen die hebben geleid tot de vaststelling van richtlijn 2006/52/EG en dus ook van deze regeling, zijn hieronder uiteengezet.
Levensmiddelenadditieven kunnen alleen voor gebruik in levensmiddelen worden goedgekeurd als zij voldoen aan bijlage II bij richtlijn 89/107/EEG1 . Bij richtlijn 95/2/EG2 is een lijst van levensmiddelenadditieven vastgesteld die in de Gemeenschap mogen worden gebruikt, alsmede de voorwaarden voor het gebruik daarvan. Bij richtlijn 94/35/EG3 is een lijst van zoetstoffen vastgesteld die in de Gemeenschap mogen worden gebruikt, alsmede de voorwaarden voor het gebruik daarvan. Deze richtlijnen zijn in Nederlandse wetgeving omgezet bij de hierboven onder a en b genoemde regelingen.
Sedert de vaststelling van de richtlijnen 95/2/EG en 94/35/EG hebben zich technische ontwikkelingen op het gebied van levensmiddelenadditieven voorgedaan. Deze richtlijnen moesten aan deze ontwikkelingen worden aangepast.
Op grond van een op 26 november 2003 door de Europese Autoriteit voor voedselveiligheid (EFSA) uitgebracht advies zijn wijzigingen aangebracht in de bestaande vergunningen. Doel hiervan was het gehalte aan nitrosaminen zo laag mogelijk te houden. Dat is bereikt door de concentraties aan levensmiddelen toegevoegde nitrieten en nitraten te verlagen en tegelijk de microbiologische veiligheid van levensmiddelen te waarborgen.
De EFSA adviseerde de gehalten aan nitriet en nitraat in de wetgeving vast te leggen als ‘toegevoegde hoeveelheid’. De EFSA was van mening dat niet zozeer de resthoeveelheid als wel de toegevoegde hoeveelheid nitriet bijdraagt tot de remmende werking tegen C. botulinum. De bepalingen zijn zodanig gewijzigd dat de door de EFSA genoemde toegestane maximumconcentraties in vleesproducten die al dan niet een hittebehandeling hebben ondergaan, in kaas en in vis als toegevoegde hoeveelheden moeten worden uitgedrukt. Bij wijze van uitzondering moesten echter voor sommige traditioneel vervaardigde vleesproducten maximale restgehalten worden vastgesteld, mits de producten adequaat werden gespecificeerd en geïdentificeerd. Met de vastgestelde gehalten wordt gewaarborgd dat de aanvaardbare dagelijkse inname (ADI) die het Wetenschappelijk Comité voor de menselijke voeding in 1990 heeft vastgesteld, niet wordt overschreden.
Producten die niet specifiek in deze regeling zijn genoemd, maar die traditioneel op een soortgelijke wijze worden vervaardigd (dat wil zeggen soortgelijke producten), kunnen, indien nodig, overeenkomstig de artikelen 5 en 6 van richtlijn 95/2/EG in categorieën worden ingedeeld. Voor kaas moest het gehalte worden uitgedrukt als toegevoegde hoeveelheid in de kaasmelk. Indien een behandeling wordt toegepast waarbij toevoeging van nitraat volgt op verwijdering van wei en toevoeging van water, moest dit leiden tot gehalten die gelijk zijn aan die welke zouden zijn verkregen indien het nitraat rechtstreeks aan de kaasmelk was toegevoegd.
Op grond van richtlijn 2003/114/EG4 waren de Commissie en de EFSA verplicht de voorwaarden voor het gebruik van E 214 tot E 219 p-hydroxybenzoaten en de natriumzouten daarvan vóór 1 juli 2004 te herzien. De EFSA heeft de gegevens over de veiligheid van p-hydroxybenzoaten beoordeeld en op 13 juli 2004 advies uitgebracht. De EFSA heeft een ADI voor de hele groep vastgesteld van 0–10 mg/kg lichaamsgewicht voor de som van de methyl- en ethylester van p-hydroxybenzoëzuur en de natriumzouten daarvan.
De EFSA was van mening dat propylparaben niet in deze groep-ADI moest worden opgenomen omdat propylparaben, in tegenstelling tot methyl- en ethylparaben, bij jonge ratten gevolgen heeft voor de geslachtshormonen en de mannelijke voortplantingsorganen. Omdat er geen duidelijk ‘no-observed-adverse-effect-level’ (NOAEL) aan te wijzen was, kon de EFSA geen aanbeveling doen voor een ADI voor propylparaben. E 216 propyl-p-droxybenzoaat en E 217 propyl-p-hydroxybenzoaat, natriumzout, moesten daarom in richtlijn 95/2/EG worden geschrapt. Bovendien moest de vergunning voor het gebruik van p-hydroxybenzoaten in vloeibare voedingssupplementen worden ingetrokken.
Bij beschikking 2004/374/EG5 werd het in de handel brengen en de invoer van geleiproducten in minicups die gelvormende levensmiddelenadditieven op basis van zeewier of bepaalde gomsoorten bevatten, opgeschort omdat bij deze producten verstikkingsgevaar bestaat. In het licht van een herziening van die beschikking moest het gebruik van bepaalde gelvormende levensmiddelenadditieven in geleiproducten in minicups worden uitgesloten.
Het Wetenschappelijk Comité voor de menselijke voeding heeft de gegevens over de veiligheid van erytritol beoordeeld en op 5 maart 2003 advies uitgebracht. Het comité kwam tot de conclusie dat het gebruik van erytritol als levensmiddelenadditief aanvaardbaar is. Het comité wees er ook op dat erytritol een laxerende werking heeft, maar bij een hogere dosis dan andere polyolen. Erytritol heeft vele niet-zoetende technologische eigenschappen die in een groot aantal levensmiddelen – van suikerwaren tot zuivelproducten – een belangrijke rol spelen. Erytritol fungeert onder andere als smaakversterker, draagstof, bevochtigingsmiddel, stabilisator, verdikkingsmiddel, vulstof en complexvormer. Het gebruik van erytritol moest worden toegestaan voor dezelfde toepassingen bij levensmiddelen als de andere momenteel toegelaten polyolen.
Daarnaast moest richtlijn 94/35/EG worden gewijzigd aangezien erytritol, net als de andere momenteel toegelaten polyolen, ook als zoetstof kan worden gebruikt. Dit heeft geleid tot een aanpassing van de Warenwetregeling Gebruik van zoetstoffen in levensmiddelen bij artikel II van deze regeling. Artikel II kan echter pas in werking treden nadat erytritol bij het Warenwetbesluit Zoetstoffen is toegelaten als zoetstof.
Het Wetenschappelijk Comité voor de menselijke voeding heeft de gegevens over de veiligheid van hemicellulose van soja beoordeeld en op 4 april 2003 advies uitgebracht. Het comité kwam tot de conclusie dat het gebruik van hemicellulose van soja in bepaalde levensmiddelen ten aanzien waarvan het advies was gevraagd, en in bepaalde concentraties, aanvaardbaar is. Daarom diende dergelijk gebruik voor bepaalde doeleinden te worden toegestaan. Om een en ander te vergemakkelijken voor personen die aan een allergie lijden, mocht dergelijk gebruik echter niet worden toegestaan voor onbewerkte levensmiddelen waarin men niet verwacht soja aan te treffen. Wanneer een product van sojabonen vervaardigde hemicellulose bevat, moet de consument hier in elk geval over geïnformeerd worden overeenkomstig richtlijn 2000/13/EG6 . Deze richtlijn is in Nederlandse wetgeving omgezet bij het Warenwetbesluit Etikettering van levensmiddelen (WEL).
De EFSA heeft de gegevens over de veiligheid van ethylcellulose beoordeeld en op 17 februari 2004 advies uitgebracht. De EFSA heeft besloten ethylcellulose op te nemen in de door het Wetenschappelijk Comité voor de menselijke voeding ingestelde groep ‘geen ADI vastgesteld’ voor gemodificeerde celluloses. Ethylcellulose wordt voornamelijk toegepast in voedingssupplementen en ingekapselde aroma’s. Het gebruik van ethylcellulose moest derhalve op dezelfde wijze worden toegestaan als voor andere celluloses.
De EFSA heeft de gegevens over de veiligheid van pullulan beoordeeld en op 13 juli 2004 advies uitgebracht. De EFSA achtte het gebruik van pullulan aanvaardbaar in de oppervlaktelaag van voedingssupplementen in de vorm van capsules en tabletten en in ademverfrissers in de vorm van dunne blaadjes. Deze gebruikswijzen dienden derhalve te worden toegestaan.
De EFSA heeft de gegevens over de veiligheid van tert-butylhydrochinon (TBHQ) beoordeeld en op 12 juli 2004 advies uitgebracht. De EFSA heeft een ADI van 0-0,7 mg/kg lichaamsgewicht vastgesteld voor dit antioxidant en geconcludeerd dat het gebruik ervan in bepaalde concentraties in bepaalde levensmiddelen aanvaardbaar zou zijn. Dit additief diende derhalve te worden toegestaan.
Het Wetenschappelijk Comité voor de menselijke voeding heeft de gegevens over de veiligheid van zetmeelaluminiumoctenylsuccinaat beoordeeld en op 21 maart 1997 advies uitgebracht. Het Comité concludeerde dat het gebruik van dit additief als onderdeel van micro-ingekapselde vitaminen en carotenoïden als aanvaardbaar te beschouwen is. Dit gebruik diende derhalve te worden toegestaan.
Tijdens de vervaardiging van zuremelkse kaas wordt aan de gepasteuriseerde melk E 500ii natriumwaterstofcarbonaat toegevoegd om de door melkzuur veroorzaakte zuurtegraad te bufferen tot een geschikte pH-waarde en zo de nodige groeicondities te creëren voor de rijpingscultures. Daarom diende het gebruik van natriumwaterstofcarbonaat in zuremelkse kaas te worden toegestaan.
Vóór de inwerkingtreding van deze regeling was het toegestaan een mengsel van sorbaten (E 200, E 202 en E 203) en benzoaten (E 210 tot E 213) te gebruiken voor de conservering van gekookte garnalen. Die vergunning moest worden uitgebreid tot het gebruik ervan in alle gekookte schaal- en weekdieren.
E 551 siliciumdioxide is bij een maximumconcentratie van 5% toegestaan als draagstof voor levensmiddelenkleurstoffen. Het gebruik van siliciumdioxide als draagstof voor de levensmiddelenkleurstoffen E 171 titaandioxide en E 172 ijzeroxiden en -hydroxiden moest ook worden toegestaan bij een maximumconcentratie van 90% in verhouding tot het pigment.
Richtlijn 95/2/EG beperkt het gebruik van de in bijlage I bij die richtlijn vermelde additieven in traditioneel Frans brood ‘Pain courant français’. Dezelfde beperking moest ook gelden voor vergelijkbaar traditioneel Hongaars brood. Ook diende het gebruik van ascorbinezuur (E 300), natriumascorbaat (E 301) en calciumdinatrium-EDTA (E 385) in Hongaarse leverpastei te worden toegestaan.
De oude bepalingen inzake het gebruik van sulfieten (E 220 tot en met 228) in gekookte schaaldieren, tafeldruiven en verse lychees, moesten worden geactualiseerd.
Ingevolge een verzoek van een lidstaat en het advies van het Wetenschappelijk Comité voor de menselijke voeding van 5 maart 2003 moest 4-hexylresorcinol, dat overeenkomstig richtlijn 89/107/EEG op nationaal niveau was toegelaten, op communautair niveau worden toegelaten.
Tot slot moest de in richtlijn 95/2/EG gehanteerde terminologie worden aangepast aan die van richtlijn 89/398/EEG7 , richtlijn 2002/46/EG8 en van richtlijn 1999/21/EG9 van de Commissie van 25 maart 1999 betreffende dieetvoeding voor medisch gebruik (3). Deze wijzigingen zijn doorgevoerd in beide hierboven onder a en b genoemde Warenwetregelingen.
Voor de toepassing van deze regeling geldt een zeer ruim overgangsregime. Vanaf de inwerkingtreding van deze regeling (artikel I: met ingang van de tweede dag na publicatie in de Staatscourant; artikel II: met ingang van 1 februari 2007) mag onmiddellijk gebruik worden gemaakt van de nieuwe mogelijkheden van de gewijzigde regelgeving. Vóór 15 augustus 2008 in de handel gebrachte of geëtiketteerde producten die niet aan deze regeling voldoen (maar wel aan de ‘oude’ regelgeving), mogen evenwel worden verkocht zolang de voorraad strekt.
Overigens treedt artikel II van deze regeling niet ‘direct’ in werking, aangezien via een wijziging van het Warenwetbesluit Zoetstoffen erytritol eerst nog moet worden toegelaten als zoetstof in levensmiddelen.
In onderstaande tabel is het verband weergegeven tussen richtlijn 2006/52/EG en deze regeling.
Richtlijn 2006/52/EG | Deze regeling |
|---|---|
artikel 1, eerste lid | artikel I, onder A |
artikel 1, tweede lid | – (geen implementatie vereist) |
artikel 1, derde lid | artikel I, onder B tot en met F |
artikel 2 | artikel II |
artikel 3, eerste lid | artikel IV |
artikel 3, tweede lid | opschrift en deze transponeringstabel |
artikelen 4 en 5 | – (geen implementatie vereist) |
Bijlage I | |
1.a | artikel I.B.1 |
1.b | artikel I.B.2 |
2.a | artikel I.C.1 |
2.b | artikel I.C.2 |
2.c | artikel I.C.3 |
3.a.i | artikel I.D.1 |
3.a.ii. 1° streepje | artikel I.D.2 |
3.a.ii. 2° streepje | artikel I.D.3 |
3.a.ii. 3° streepje | artikel I.D.4 |
3.b. 1° streepje | artikel I.D.5 |
3.b. 2° streepje | artikel I.D.6 |
3.b. 3° streepje | artikel I.D.7 |
3.c | artikel I.D.8 |
3.d.i | artikel I.D.9.a |
3.d.ii | artikel I.D.9.b |
3.d.iii | artikel I.D.9.c |
4.a | artikel I.D.10.a |
4.b | artikel I.D.10.b |
4.c | artikel I.D.10.c |
4.d, e, f | artikel I.D.10.d |
4.g | artikel I.D.10.f |
4.h | artikel I.D.10.e |
4.i | artikel I.D.10.g |
4.j | artikel I.D.10.h |
5.a | artikel I.E.1 |
5.b | artikel I.E.2 |
5.c | artikel I.E.3 |
6.a | artikel I.F.1 |
6.b | artikel I.F.2 en 3 |
6.c | artikel I.F.4 |
Bijlage II | |
1. | artikel II.1 |
2. | artikel II.2 |
Deze regeling heeft geen gevolgen voor de administratieve lasten voor de burger en het bedrijfsleven.
De Minister van Volksgezondheid, Welzijn en Sport,
J.F. Hoogervorst
Stcrt. 1996, 186; laatstelijk gewijzigd bij regeling van 12 januari 2005, Stcrt. 12.
Kopieer de link naar uw clipboard
https://zoek.officielebekendmakingen.nl/stcrt-2006-220-p32-SC77604.html
De hier aangeboden pdf-bestanden van het Staatsblad, Staatscourant, Tractatenblad, provinciaal blad, gemeenteblad, waterschapsblad en blad gemeenschappelijke regeling vormen de formele bekendmakingen in de zin van de Bekendmakingswet en de Rijkswet goedkeuring en bekendmaking verdragen voor zover ze na 1 juli 2009 zijn uitgegeven. Voor pdf-publicaties van vóór deze datum geldt dat alleen de in papieren vorm uitgegeven bladen formele status hebben; de hier aangeboden elektronische versies daarvan worden bij wijze van service aangeboden.
