Kamerstuk
| Datum publicatie | Organisatie | Vergaderjaar | Dossier- en ondernummer |
|---|---|---|---|
| Tweede Kamer der Staten-Generaal | 2014-2015 | 29477 nr. 294 |
Zoals vergunningen, bouwplannen en lokale regelgeving.
Adressen en contactpersonen van overheidsorganisaties.
U bent hier:

| Datum publicatie | Organisatie | Vergaderjaar | Dossier- en ondernummer |
|---|---|---|---|
| Tweede Kamer der Staten-Generaal | 2014-2015 | 29477 nr. 294 |
Vastgesteld 19 september 2014
De vaste commissie voor Volksgezondheid, Welzijn en Sport heeft een aantal vragen en opmerkingen voorgelegd aan de Minister van Volksgezondheid, Welzijn en Sport over de brief van 11 juni 2014 over de ontwerpregeling tot wijziging van de bijlage bij de Regeling maximumprijzen geneesmiddelen (Kamerstuk 29 477, nr. 288).
De vragen en opmerkingen zijn op 25 juni 2014 aan de Minister van Volksgezondheid, Welzijn en Sport voorgelegd. Bij brief van 18 september 2014 zijn ze door hem beantwoord.
De voorzitter van de commissie, Neppérus
De griffier van de commissie, Teunissen
De leden van de fracties van de PvdA en de SP hebben mij op 25 juni 2014 vragen en opmerkingen voorgelegd over maximumprijzen voor geneesmiddelen (Wgp) en de verenigbaarheid van prijsmaatregelen voor geneesmiddelen met het Europese recht. Ik dank de leden van deze fracties voor hun inbreng en geef hieronder mijn antwoord.
Voordat ik over ga tot beantwoording van de individuele vragen van de leden van de fracties van de PvdA en de SP merk ik op dat een aantal vragen niet in het gevraagde detail is te beantwoorden. Daarnaast kan ik geen volledig uitsluitsel geven over vragen ten aanzien van de verenigbaarheid van prijsmaatregelen met het Europese recht. Dat oordeel is immers voorbehouden aan de Europese rechter. Voor een dergelijke beoordeling is ook meer duidelijkheid nodig over de te beoordelen (concrete) prijsmaatregel zelf, de context waarbinnen de maatregel geldt en vooral hoe de maatregel feitelijk uitwerkt. In het licht van het bovenstaande zijn de vragen dan ook deels in meer algemene bewoordingen beantwoord.
Inbreng van de fractie van de PvdA
De leden van de fractie van de PvdA merken op dat zij met interesse kennis hebben genomen van de Ontwerpregeling tot 35e wijziging van de bijlage bij de Regeling maximumprijzen geneesmiddelen. Zij zijn erg benieuwd naar het aantal bespaarde euro’s en het percentage gerealiseerde kostenreductie als gevolg van de wijziging van de maximumprijzen van geneesmiddelen. Zij verzoeken aan te geven wat de laatste tien wijzigingen per keer hebben opgeleverd. Zij vragen ook in hoeverre ik tevreden ben over de tot nu toe behaalde besparingen.
Bij het vaststellen van maximumprijzen op basis van de Wet Geneesmiddelenprijzen (Wgp) gaat het om brutoapotheekinkoopprijzen. Dat zijn meestal niet de prijzen die gedeclareerd worden. De daadwerkelijk door apothekers of zorgverzekeraars uitonderhandelde en gedeclareerde prijzen zijn over het algemeen lager dan de brutoapotheekinkoopprijzen. Daarnaast wordt de prijsvorming van geneesmiddelen door het preferentiebeleid en ander inkoopbeleid van zorgverzekeraars beïnvloed.
Zoals ook is aangegeven in het op 5 juli 2012 aan de Tweede Kamer toegezonden rapport van Conquaestor over de werking en de toekomstbestendigheid van de Wet geneesmiddelenprijzen, is het daarom niet goed mogelijk om behaalde besparingen specifiek toe te wijzen aan onderscheiden beleidsmaatregelen van zowel de overheid als zorgverzekeraars»1. Het aantal «bespaarde euro’s» op grond van verlaging van Wgp-maximumprijzen is dan ook niet één op één af te leiden uit een daling van de Wgp-maximumprijzen en het bijbehorende volume. Wel is in het rapport van Conquaestor een meer algemene schatting gemaakt van de «opbrengst» van de Wgp:
«Op basis van brutoprijzen is wel een schatting gemaakt. De opbrengst van de Wgp kan worden geschat op tussen de € 800 miljoen en € 1.200 miljoen per jaar in 2010. Een inschatting op het niveau van uitonderhandelde nettoprijzen zal lager uitvallen. Per jaar neemt het berekende kostenverlagingeffect toe doordat het volume van geneesmiddelen toeneemt en de brutoprijzen onder andere onder invloed van de Wgp blijven dalen. Het jaarlijkse kostenverlagingeffect van de Wgp is toegenomen van ongeveer hfl. 700 miljoen in 1996 tot ongeveer € 1.000 miljoen in 2010.»
Voor een meer uitgebreide verhandeling en de bij de schatting gehanteerde aannames verwijs ik naar Hoofdstuk 5 van het rapport van Conquaestor (blz. 51 t/m 54).
Het Zorginstituut Nederland (ZIN) heeft in de GIPeiling 2012 van september 2013 een meer actuele inschatting gemaakt van de opbrengsten van de Wgp2.
|
2004 |
2005 |
2006 |
2007 |
2008 |
2009 |
2010 |
2011 |
2012 |
2013 voorlopig |
|
|---|---|---|---|---|---|---|---|---|---|---|
|
Clawback |
180,8 |
182,0 |
187,4 |
206,1 |
130,6 |
201,5 |
191,9 |
159,2 |
152,5 |
141,0 |
|
Prijsdruk WGP |
– 7,1 |
65,3 |
271,4 |
522,3 |
868,3 |
1.242,8 |
1.633,6 |
1.894,3 |
1.938,0 |
2.200,4 |
|
Overige prijsverlagingen |
411,4 |
452,0 |
435,6 |
354,2 |
296,4 |
246,5 |
168,4 |
201,7 |
374,5 |
343,5 |
|
Prijsverlagingen door preferentiebeleid |
191,4 |
373,4 |
520,5 |
593,8 |
693,4 |
719,9 |
||||
|
Totale cumulatieve prijsdruk |
585,1 |
699,3 |
894,4 |
1.082,6 |
1.486,7 |
2.064,2 |
2.514,4 |
2.849,1 |
3.158,4 |
3.404,7 |
Alle bedragen inclusief 6% BTW 1 = 1 miljoen euro
Bron: GIP/Zorginstituut Nederland
Ik ben tevreden over het samenspel van de Wgp met de overige beleidsmaatregelen (waaronder door de overheid af te sluiten prijsarrangementen) en de inzet van zorgverzekeraars. De Wgp doet wat met de Wgp is beoogd: de wet bewerkstelligt apotheekinkoopprijzen op een gemiddeld Europees niveau. Dat blijk uit het al eerder aangehaald onderzoek naar de werking en de toekomstbestendigheid van de Wgp dat is uitgevoerd door Conquaestor.
Wel zijn de nadelen als zodanig van referentieprijssystemen en van het uitbreiden van prijsreferentiesystemen in Europa en daarbuiten een punt van aandacht. Hiervoor heb ik in de brieven aan de Tweede Kamer van 19 mei 2011 en 31 mei 2013 aandacht gevraagd mede in verband met de toegankelijkheid van geneesmiddelen in minder welvarende landen3.
Genoemde leden vragen in hoeverre de berekening van maximumprijzen voor geneesmiddelen, indien deze plaats zou vinden conform het Noorse systeem (uitbereiding naar tien referentielanden) en met de Noorse rekenmethode (maximumprijzen op basis van de drie goedkoopste referentielanden), in strijd zou zijn met Europees recht. Welke concrete belemmeringen ziet de Minister ten aanzien van respectievelijk de Transparantierichtlijn 89/105/EEG, het Verdrag betreffende de werking van de Europese Unie en de Ontwerprichtlijn die de Transparantierichtlijn op termijn zal gaan vervangen? Waarop is de overtuiging gebaseerd dat een dergelijke wijziging werkelijk tot overtreding van Europese regels zou leiden? Welke voorbeelden zijn daarvan bekend? Hoe zouden deze belemmeringen opgelost kunnen worden?
Welke andere potentiële belemmeringen ten aanzien van Europees recht ziet de Minister?
Ik kan geen uitsluitsel geven of de voorgestelde berekening en de uitwerking daarvan in strijd zouden zijn met het Europese recht. Enerzijds is die taak voorbehouden aan de Europese rechter en anderzijds ontbreekt de daarvoor benodigde detailkennis van de uitwerking van de prijsmaatregel en van het Noorse systeem. Evenals de context waarbinnen de maatregel is afgekondigd en hoe de maatregel feitelijk uitwerkt. Dit zijn alle elementen die bij een toets of er sprake is van strijd met het Europese recht aan de orde komen.
Uitgangspunt bij de toetst naar de verenigbaarheid met het Europese recht vormt het feit dat er sprake is van een interne markt voor geneesmiddelen. Dat betekent dat geneesmiddelen die rechtmatig in de handel zijn gebracht in een Lid-Staat van de EU verhandeld moeten kunnen worden naar andere Lid-Staten en daar met redelijke winst moeten kunnen worden afgezet.
Daarnaast mag er geen onderscheid naar de herkomst van geneesmiddelen worden gemaakt.
In de memorie van toelichting op de Wgp is ten aanzien van de verenigbaarheid met het Europese recht aangegeven:
«Prijsbeheersingsmaatregelen zijn als zodanig dus niet verboden onder artikel 30 van het EG-verdrag. Van een Maatregel van Gelijke Werking (MGW) is volgens de jurisprudentie van het Hof pas sprake wanneer de prijzen op een zodanig niveau worden vastgesteld dat de afzet van ingevoerde producten onmogelijk wordt gemaakt of meer bemoeilijkt wordt dan de afzet van nationale producten. Wanneer een prijscontrolesysteem wel onderscheid maakt tussen nationale en ingevoerde producten, beschouwt het Hof die maatregel als een MGW indien dit de verkoop van geïmporteerde producten op enigerlei wijze kan belemmeren. In dit verband wordt gewezen op het arrest van het Hof van Justitie van de Europese Gemeenschappen van 19 maart 1991 in de zaak C-249/88, Commissie van de Europese Gemeenschappen contra het Koninkrijk België. In dit arrest worden o.a. de grieven van de Commissie inzake de vaststelling van maximumprijzen voor farmaceutische producten en de uit de toepassing van de regeling voortvloeiende prijsniveaus door het Hof afgewezen. Het Hof formuleerde in dit arrest dat van een MGW sprake is wanneer ingevoerde producten niet met redelijke winst op de markt van de invoerende staat kunnen worden afgezet. Als bewijs dat van een dergelijke situatie sprake is kan naar het oordeel van het Hof echter niet worden beschouwd het feit dat importeurs ervan hebben afgezien producten uit andere lidstaten in de handel te brengen wegens het te lage niveau van de toegestane prijzen».
In essentie zijn de uitgangspunten voor de toets van verenigbaarheid van overheidsmaatregelen met de verenigbaarheid met het Europese recht niet gewijzigd.
De huidige Transparantierichtlijn (89/105/EEG), is vastgesteld in de verwachting dat het nationale prijs- en vergoedingenmaatregelen van Lid-Staten om de uitgaven voor de zorg te controleren, de werking van de interne markt negatief zouden beïnvloeden. De Transparantierichtlijn beoogt daarom de transparantie van (de totstandkoming van) de maatregelen van Lid-Staten tot prijscontrole en vergoeding van geneesmiddelen. De richtlijn geeft een aantal procedurele eisen waarmee belanghebbenden in staat worden gesteld om na te gaan dat nationale prijs en vergoedingsmaatregelen geen obstakels vormen voor handel in geneesmiddelen in de Europese Unie in overeenstemming met artikel 28 van het EU verdrag. Zo zullen dergelijke maatregelen bijvoorbeeld gebaseerd moeten zijn op vooraf kenbare objectieve criteria. Zo vormt de wens om een bepaald bedrag aan uitgaven te besparen niet een dergelijke objectief criterium. De bepalingen van de richtlijn hebben slechts invloed op nationaal prijs- en vergoedingsbeleid en de organisatie van de sociale zekerheid voor zover nodig om transparantie te bereiken.
Het Hof van Justitie van de EU heeft ten aanzien van de implementatie en de interpretatie van de Transparantierichtlijn meer recent de volgende arresten gewezen:
Zaak C-424/99, 27 november 2001, Commissie v. Oostenrijk
Zaak C-229/00, 12 juni 2003, Commissie v. Finland
Zaak C-245/03, 20 januari 2005, Merck, Sharp & Dohme
Zaak C-296/03, 20 januari 2005, GlaxoSmithKline
Zaak C-317/05, 26 oktober 2006, Pohl-Boskamp
Zaak C-311/07, 17 juli 2008, Commissie v. Oostenrijk
Zaak C-352/07, 2 april 2009, Menarini and gevoegde zaken C-353/07 tot C-356/07, C-365/07 tot C-367/07 en C-400/07
De eerste zes arresten hebben met name betrekking op de opname van geneesmiddelen onder de werkingssfeer van nationale stelsels van ziektekostenverzekering. Het laatste arrest ziet op de prijsvorming met betrekking tot geneesmiddelen en de mogelijkheden tot het bevriezen en verlagen van geneesmiddelenprijzen.
De leden van de fractie van de PvdA vragen hoe de Minister de beschikking krijgt over prijslijsten van de huidige referentielanden. Kan zij op soortgelijke wijze prijslijsten verkrijgen van bijvoorbeeld Denemarken, Ierland, Finland, Noorwegen, Oostenrijk en Zweden? Zo ja, welke startkosten zou dat precies met zich meebrengen? Zo nee, waarom niet? Bij welke instanties zouden de bedoelde prijzen opgevraagd kunnen worden? Op welke wijze verzamelt Noorwegen haar prijslijsten van referentielanden en is er een reden waarom Nederland dat niet op dezelfde manier zou kunnen doen? Tot welk theoretisch probleem zou dit voor Nederland kunnen leiden?
Bij de vaststelling van de maximumprijzen wordt gebruik gemaakt van algemeen aanvaarde prijslijsten in de referentielanden (zie de Regeling referentieprijslijsten geneesmiddelen). De prijsgegevens worden gekocht van de desbetreffende leveranciers van prijslijsten. Op dit moment zijn dat de prijslijsten die zijn uitgegeven door:
Algemene Pharmaceutische Bond (België)
Informationsstelle für Arzneispezialitäten (Duitsland)
Société d'Éditions Medico-pharmaceutiques (Frankrijk)
Dictionary of Medicines and Devices (Verenigd Koninkrijk)
De prijsgegevens dienen door middel van een geautomatiseerd gegevensbestand ter beschikking te worden gesteld. De bestanden moeten prijzen bevatten op apotheekinkoopniveau dan wel moeten de desbetreffende prijzen terug te rekenen zijn naar apotheekinkoopprijzen. Daarnaast dient de technische indeling van geneesmiddelen zodanig te zijn dat een indeling kan worden gemaakt van gelijke geneesmiddelen in de zin van de WGP waarbij wordt uitgegaan van geneesmiddelen met een gelijke werkzame stof, farmaceutische vorm en sterkte. Voor de berekening van maximumprijzen is het daarnaast nodig dat er gegevens beschikbaar zijn waardoor de volgende stappen kunnen worden doorlopen:
1. Voor ieder referentieland worden de vergelijkbare geneesmiddelen in een productgroep ingedeeld.
2. Per land wordt op basis van de merkstamnaam van het desbetreffende vergelijkbare geneesmiddel de verpakkingsgrootte(n) met de laagste prijs per eenheid product geselecteerd.
3. Als de geselecteerde verpakkingsgrootte(n) van dat geneesmiddel een aantal malen in de prijslijst staat, wordt/worden de gemiddelde prijs/prijzen van deze verpakkingsgrootte(n) in de berekening betrokken.
4. Per land worden de prijzen van de geselecteerde verpakkingen gemiddeld.
5. Indien nodig wordt de gemiddelde prijs omgerekend in euro’s. Bij de omrekening naar euro’s wordt uitgegaan van de middenkoers die geldt op de datum waarop de als uitgangspunt genomen prijslijst is uitgegeven.
6. De maximumprijs wordt vastgesteld op het rekenkundig gemiddelde van de (omgerekende) gemiddelden van de referentielanden.
Ik beschik niet over gegevens of er in de door de leden van de fractie van de PvdA genoemde landen algemeen aanvaardbare prijslijsten beschikbaar zijn die voldoen aan de hierboven genoemde voorwaarden. En zo ja of die prijslijsten ter beschikking zullen worden gesteld met als doel om maximumprijzen in Nederland vast te stellen en welke (start)kosten daaraan verbonden zouden zijn.
Tot slot vragen de leden van de fractie van de PvdA hoeveel additionele uitvoeringskosten uitbereiding van de berekening van maximumprijzen naar tien referentielanden betekent. Hoeveel eventuele additionele uitvoeringskosten verwacht de Minister per berekening bij het meenemen van de prijslijsten van eerder genoemde landen? Op welke gegevens en aannames baseert de Minister dit? Indien de berekening via het Noorse systeem en de Noorse rekenmethode twee keer per jaar plaatsvindt, stijgen de additionele uitvoeringskosten dan proportioneel mee of kan de tweede berekening in hetzelfde jaar tegen lagere additionele uitvoeringskosten plaatsvinden? Graag ontvangen deze leden een uitgebreide berekening van deze meerkosten.
Gezien het ontbreken van de daarvoor benodigde gegevens is het niet goed mogelijk om aan te geven welke additionele uitvoeringskosten gemoeid zijn met een uitbreiding van de berekening van maximumprijzen naar tien referentielanden en hoeveel eventuele additionele uitvoeringskosten er verwacht kunnen worden per berekening bij het meenemen van de prijslijsten van de eerder genoemde landen. Elke aanname en elk bedrag dat ik op dit moment zou noemen, zou een slag in de lucht zijn.
Inbreng van de fractie van de SP
De leden van de SP-fractie hebben kennisgenomen van de brief van de Minister. Zij vragen opheldering van de Minister met betrekking tot de onderstaande punten.
De leden van de SP-fractie vragen de Minister of zij inzicht heeft in de gemiddelde prijsontwikkeling, en of er daarbij sprake is van een prijsstijging, -daling of -stabilisering. Hoe verklaart de Minister deze ontwikkelingen? Ook vragen zij in hoeverre de Minister invloed kan uitoefenen op deze ontwikkeling, en of zij daartoe bereid is. Deze leden verwachten een uitgebreide toelichting.
Er bestaat inderdaad inzicht in de gemiddelde prijsontwikkeling op apotheekinkoopniveau. De apotheekinkoopprijzen zijn meestal niet de prijzen die gedeclareerd worden en dus onderdeel uitmaken van de uitgaven voor farmaceutische zorg. De daadwerkelijk door apothekers of zorgverzekeraars uitonderhandelde en gedeclareerde prijzen zijn over het algemeen lager.
Er is sprake van een daling van de gemiddelde apotheekinkoopprijzen. De oorzaken daarvan zijn gelegen in de werking van de Wet geneesmiddelenprijzen, het preferentiebeleid, het uit octrooi lopen van geneesmiddelen waardoor er generieke, meestal lager geprijsde, geneesmiddelen ter beschikking komen en het inkoopbeleid van zorgverzekeraars. Met de Wet geneesmiddelenprijzen worden de apotheekinkoopprijzen vastgesteld op het gemiddelde van de prijzen in de referentielanden. Dalen de apotheekinkoopprijzen in de referentielanden dan dalen de Nederlandse maximumprijzen eveneens. De Nederlandse maximum-apotheekinkoopprijzen worden twee keer per jaar geactualiseerd.
De Stichting farmaceutische kengetallen (SFK) heeft berekend dat de geneesmiddelenprijzen (op apotheekinkoopniveau) sinds 2007 gemiddeld met 33,9% zijn gedaald. De SFK drukt de ontwikkeling van het prijspeil van geneesmiddelen uit in een index. De SFK bepaalt op maandbasis de verhouding tussen de totale kosten van de door openbare apotheken verstrekte geneesmiddelen en de kosten van dezelfde hoeveelheid van dezelfde middelen tegen de prijzen van de daaropvolgende maand. Wijzigingen in aard en hoeveelheid van de verstrekte geneesmiddelen hebben daardoor geen invloed op de index.
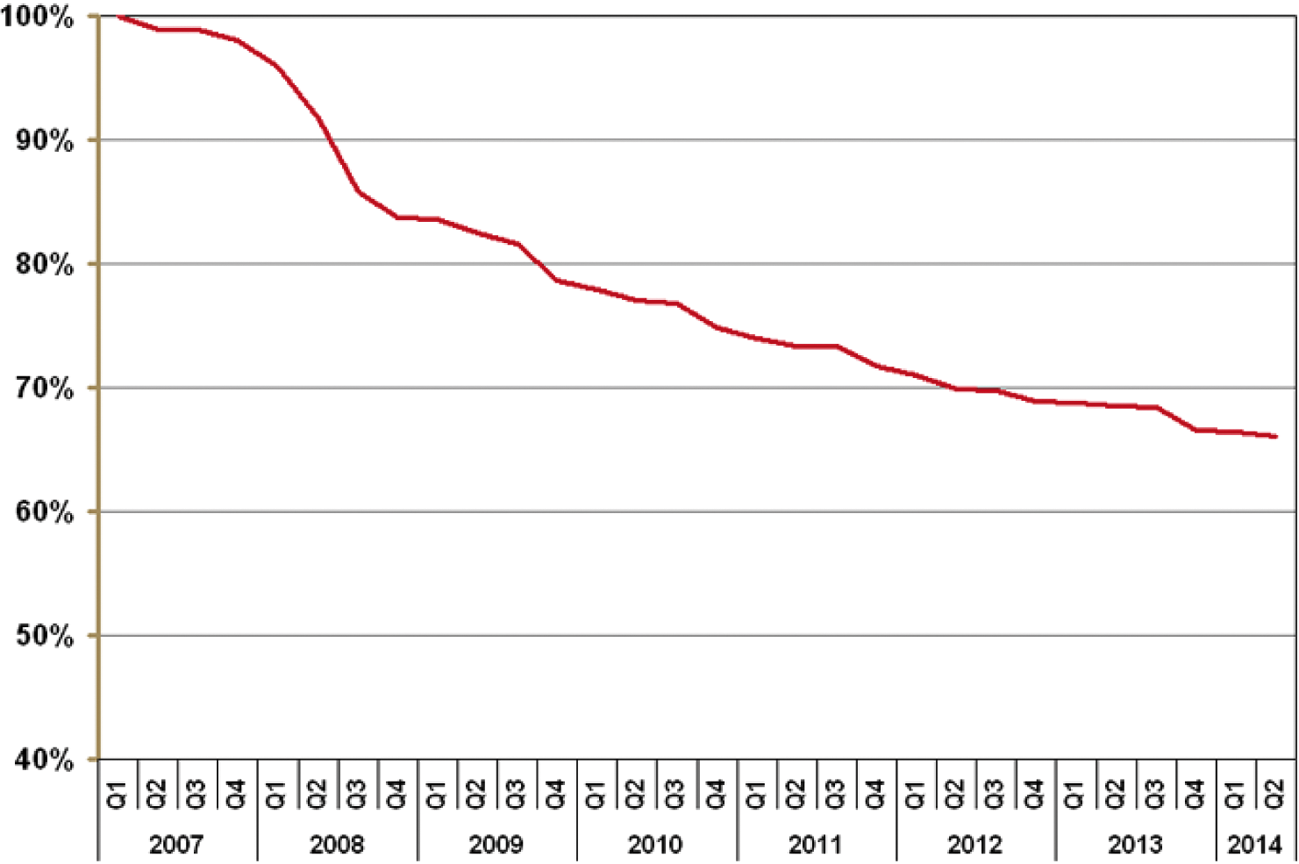
De geneesmiddelprijzen zijn sinds 2007 gemiddeld met 33,9% gedaald.
Kortheidshalve verwijs ik de leden van de fractie van de SP ook naar de eerder aangehaalde in september 2013 gepubliceerde GIPeilingen 2012 van het Zorginstituut Nederland (ZIN) waarin ook de oorzaken van prijsdalingen zijn aangegeven.
De leden van de SP-fractie zijn bekend met het systeem waarbij maximumprijzen voor geneesmiddelen gebaseerd worden op de prijzen in de ons omringende referentielanden. Zij herinneren de Minister er graag aan dat in bijvoorbeeld Denemarken medicijnen centraal ingekocht worden. Zij constateren dat de Denen per hoofd van de bevolking aanzienlijk minder betalen voor medicijnen dan Nederlanders. Hoe verklaart de Minister dit grote verschil? Is de Minister bereid te onderzoeken wat de besparing is voor Nederland, indien overgestapt wordt op dit systeem? Zo nee, dan willen zij graag weten waarom niet, en in wiens belang dit is. Zij verwachten een uitgebreide toelichting.
Ik ben niet bereid om te onderzoeken wat de geschatte besparing zou zijn als Nederland overstapt naar een systeem van centrale inkoop. Een dergelijk onderzoek is bewerkelijk en zal niet meer dan een theoretische exercitie zijn zonder praktische waarde binnen ons zorgstelsel. Daarnaast zijn de vergelijkingen van de uitgaven per hoofd van bevolking in de verschillende landen onzuiver omdat bijvoorbeeld de uitgaven voor de verstrekkingen van dure geneesmiddelen in een aantal landen tot het ziekenhuisbudget behoren en in een aantal andere landen niet, zoals aangegeven in de recente publicatie van de SFK: «Medicijnuitgaven dalen in Nederland sterker dan in West-Europa» (7 augustus 2014, Pharmaceutisch Weekblad, Jaargang 149 Nr 32/33).
De leden van de SP-fractie zijn van mening dat een berekening van de maximumprijzen op basis van het Noorse model vele honderden miljoenen euro’s kan besparen. In plaats van uit te gaan van het gemiddelde van vier referentielanden en daarvan het gemiddelde te nemen, wordt er daarbij uitgegaan van negen landen, en per medicijn wordt vervolgens het gemiddelde van de drie laagste brutoprijzen aangehouden. Is de Minister bereid te onderzoeken wat het bepalen van maximumprijzen volgens het beschreven systeem de Nederlandse belastingbetaler bespaart? Zo nee, waarom niet? Zij verwachten een uitgebreid antwoord op de gestelde vragen.
Allereerst merk ik op dat reeds een initiatief-wetsvoorstel van het lid Kuzu (PvdA) tot wijziging van de Wgp aanhangig is bij de Tweede Kamer, waarmee wordt beoogd het Noorse model voor het vaststellen van maximumprijzen te introduceren. Daarnaast gaat het bij het vaststellen van
maximumprijzen op basis van de Wet Geneesmiddelenprijzen (Wgp) om brutoapotheek-inkoopprijzen. Dat zijn meestal niet de prijzen die gedeclareerd worden. De daadwerkelijk door apothekers of zorgverzekeraars uitonderhandelde en gedeclareerde prijzen zijn over het algemeen lager dan de brutoapotheekinkoopprijzen. Ook wordt de prijsvorming van geneesmiddelen door het preferentiebeleid en ander inkoopbeleid van zorgverzekeraars beïnvloed. In de antwoorden op vragen van de leden van de fractie van de PvdA en in het al aangehaalde rapport van Conquaestor over de werking en de toekomstbestendigheid van de Wet geneesmiddelenprijzen, is aangegeven dat het niet goed mogelijk is om behaalde besparingen specifiek toe te wijzen aan onderscheiden beleidsmaatregelen van zowel de overheid als zorgverzekeraars. Het aantal «bespaarde euro’s» op grond van verlaging van Wgp-maximumprijzen is dan ook niet één op één af te leiden uit een daling van de Wgp-maximumprijzen en het bijbehorende volume.
Blz. 8: «Het kostenverlagingeffect van de Wgp is niet exact te berekenen omdat een combinatie van overheidsmaatregelen en marktfactoren van invloed zijn op de uiteindelijke prijzen van en uitgaven aan geneesmiddelen».
Brief aan de Tweede Kamer van 19 mei 2011, Kamerstuk 29 248 nr. 209 en brief aan de Tweede Kamer van 31 mei 2013, Kamerstuk 29 477, nr. 245.
Kopieer de link naar uw clipboard
https://zoek.officielebekendmakingen.nl/kst-29477-294.html
De hier aangeboden pdf-bestanden van het Staatsblad, Staatscourant, Tractatenblad, provinciaal blad, gemeenteblad, waterschapsblad en blad gemeenschappelijke regeling vormen de formele bekendmakingen in de zin van de Bekendmakingswet en de Rijkswet goedkeuring en bekendmaking verdragen voor zover ze na 1 juli 2009 zijn uitgegeven. Voor pdf-publicaties van vóór deze datum geldt dat alleen de in papieren vorm uitgegeven bladen formele status hebben; de hier aangeboden elektronische versies daarvan worden bij wijze van service aangeboden.
