TOELICHTING
Algemeen
Inleiding
Om te zorgen dat voor potentieel veelbelovende interventies op snelle wijze kennis
over de effectiviteit en kosteneffectiviteit beschikbaar komt, is in 2012 het instrument
voorwaardelijke toelating tot het basispakket ingesteld. Hierbij kunnen veelbelovende
interventies (tijdelijk) gefinancierd worden uit het basispakket, op voorwaarde dat
de effectiviteit en kosteneffectiviteit in kaart worden gebracht. Door deze vormgeving
werd brede toegankelijk een vereiste. In de kamerbrief van 21 februari 2017 is door
de minister van Volksgezondheid, Welzijn en Sport het voornemen beschreven om het
huidige instrument voorwaardelijke toelating om te zetten in een subsidieregeling
waarin de knelpunten van het huidige instrument worden ondervangen.
Op 21 mei 2018 is in de Kamerbrief Subsidieregeling Veelbelovende Zorg Sneller bij
de Patiënt uitgewerkt hoe deze nieuwe subsidieregeling de problemen van de huidige
regeling zal gaan ondervangen.
Doelstelling van de subsidieregeling
De doelstelling van de regeling Veelbelovende Zorg Sneller bij de Patiënt is het versnellen
van de toegang van de patiënt tot potentieel veelbelovende zorg via opname in het
basispakket. Uitgangspunt van de Zorgverzekeringswet is dat alleen zorg die voldoet
aan ‘de stand van de wetenschap en praktijk’ tot het basispakket behoort. Met andere
woorden, alleen een interventie die als effectief t.o.v. de huidige standaard- of
gebruikelijke behandeling(en) in Nederland wordt beschouwd, maakt onderdeel uit het
Nederlandse basispakket. Via deze regeling is het mogelijk subsidie te verkrijgen
om binnen een bepaalde periode gegevens te verzamelen over de effectiviteit en kosteneffectiviteit
van een interventie t.o.v. de huidige standaard- of gebruikelijke behandeling(en).
Met de via deze regeling verkregen onderzoeksresultaten zal het Zorginstituut bepalen
of de interventie-indicatiecombinatie voldoet aan ‘de stand van de wetenschap en praktijk’.
Het Zorginstituut neemt binnen zes maanden na het indienen van de onderzoeksresultaten
een standpunt in over ‘de stand van de wetenschap en praktijk’. Als deze als positief
wordt beoordeeld, dan maakt de nieuwe interventie onderdeel uit van het verzekerde
basispakket voor de betreffende indicatie. Verder brengt het Zorginstituut bij effectieve
zorg een advies uit aan de minister voor Medische Zorg en Sport over de kosteneffectiviteit
van de interventie-indicatiecombinatie.
Achtergrond
De subsidieregeling vervangt het instrument voorwaardelijke toelating. De afgelopen
jaren zijn bij het instrument een aantal belangrijke knelpunten naar voren gekomen.
De belangrijkste knelpunten van deze regeling zijn beschreven in de Kamerbrief Herinrichting regeling voorwaardelijke pakkettoelating
1. Kernprobleem was dat bij deze regeling het proces te complex werd ervaren voor gebruikers,
met een voorbereidingsprocedure van twee jaar en veel administratieve- en juridische
verplichtingen. Concluderend bleek hieruit dat vormgeving van het versnellende instrument
via de Zorgverzekeringswet onvoldoende werkt. In de voornoemde Kamerbrief is het voornemen
aangegeven om het instrument voorwaardelijke toelating te vervangen door een beter
toegankelijke en meer effectieve subsidieregeling.
Bij het ontwerpen van de nieuwe regeling is ruime aandacht geweest voor de hulpvragen
van kleinere partijen bij het verzamelen van gegevens over de (kosten)effectiviteit.
Om de toegankelijkheid van de regeling te verbeteren, te vereenvoudigen en te versnellen
zijn ten opzichte van de regeling voor voorwaardelijke pakkettoelating veel verbeteringen
doorgevoerd:
-
• het verlagen van de toegangsdrempels voor de financiering van het onderzoek
-
• het verkorten van de voorbereidingsprocedure van tweeënhalf jaar tot circa een jaar
-
• het reduceren van administratieve stappen voor ontwikkelaars en onderzoekers in de
voorbereidingsprocedure
-
• het beperken van het onderzoek tot de voor het onderzoek benodigde patiëntenpopulatie
-
• op basis van positief beoordeeld projectidee wordt advies gegeven over de onderzoeksopzet
-
• het inschakelen van een ervaren onderzoeksconsortium, dat partijen indien nodig en
gewenst kan begeleiden bij het opzetten en uitvoeren van onderzoek
-
• het uitbreiden van de mogelijkheid tot indienen van voorstellen van eenmaal naar tweemaal
per jaar
De verwachting is dat de subsidieregeling aantrekkelijk is voor partijen die onderzoek
willen doen naar de (kosten)effectiviteit van potentieel veelbelovende interventies.
Het streven is dat op grotere schaal onderzoek van nieuwe veelbelovende zorg plaatsvindt,
waardoor deze nieuwe behandelingen en technieken snel voor de patiënt beschikbaar
komen en op kwalitatief hoogwaardiger niveau in het zorgproces worden geïntroduceerd.
Dit past in de bredere ambitie om de zorgsector te faciliteren bij het actiever en
op grotere schaal evalueren van (kosten)effectiviteit.
Motivering instrumentkeuze
Vormgeving via subsidieregeling maakt het mogelijk om de administratieve- en inhoudelijke
toegangsdrempels van financiering van zorg voor onderzoek te verlagen en om de voorbereidende
procedure substantieel te verkorten. Tevens kan de uitvoering worden beperkt van o.a.
alle zorgverzekeraars en diverse uitvoeringsinstanties tot enkel het Zorginstituut
en ZonMw.
Doordat de financiering van zorg en onderzoek in tegenstelling tot het instrument
voorwaardelijke toelating wordt beperkt tot de voor het onderzoek benodigde populatie,
ligt vormgeving van de uitvoering via de Zorgverzekeringswet niet meer voor de hand.
Daarmee wordt het ook mogelijk om de reikwijdte te verbreden naar interventies waarvan
minder gegevens over de effectiviteit beschikbaar zijn.
Tevens wordt door vormgeving via de subsidieregeling beter zichtbaar dat het om onderzoek
naar nog niet bewezen effectieve interventies gaat, in tegenstelling tot zorg in het
basispakket, waarbij de vereiste is dat deze bewezen effectief dient te zijn.
Dienst van Algemeen Economisch Belang
Er is sprake van marktfalen als het gaat om de uitvoering van een publieke taak die
door de overheid wordt opgedragen, en die niet door de markt zelf tot stand komt.
Als het gaat om onderzoek naar potentieel veelbelovende zorg kan het zijn dat er financiële
belemmeringen zijn die de totstandkoming van dit onderzoek verhinderen of vertragen,
zoals de grote omvang van de benodigde investeringen en in het geval dat de kosten
niet opwegen tegen de baten voor de ontwikkelaar. Om voor gevallen waar sprake is
van marktfalen toch het onderzoek en de hiervoor benodigde kosten te kunnen financieren
wordt een Dienst van Algemeen Economisch Belang (DAEB) gevestigd op de subsidieregeling.
Procedure van de regeling
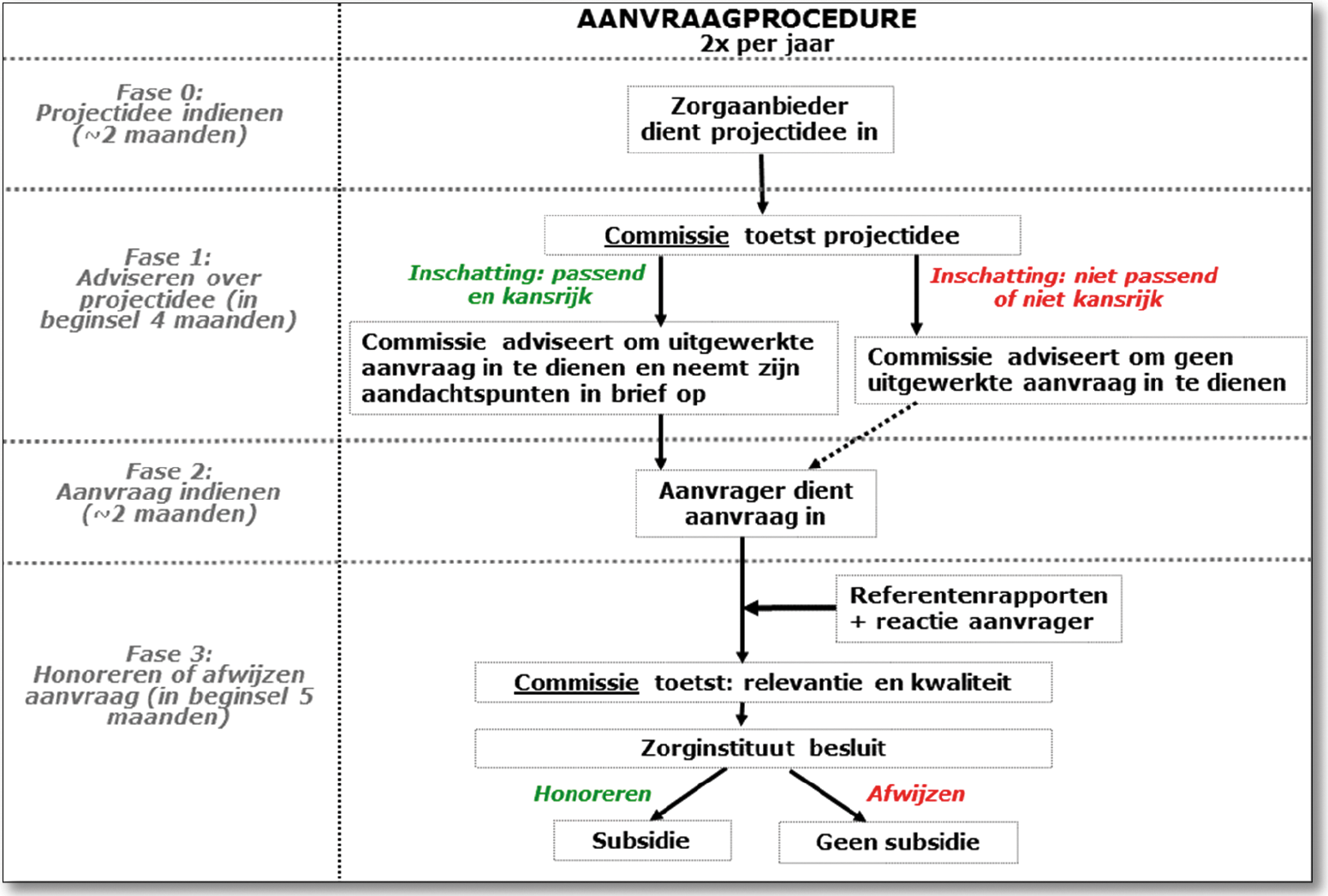
Hieronder volgt een beschrijving van de procedure van de subsidieregeling. In het
navolgende figuur is de procedure tot aan de honorering of afwijzing van een aanvraag
in grote lijnen samengevat met daaronder een toelichting voor de verschillende fases.
Fase 0 en 1: Projectidee
Een projectidee gaat vooraf aan het indienen van een subsidieaanvraag. De termijn
voor het indienen van een projectidee is in beginsel twee maanden. De tijdslijn wordt
op de website van het Zorginstituut gepubliceerd.
Het doel van deze stap is projecten te selecteren die passen binnen de regeling en
kansrijk zijn. In het projectidee beschrijft de aanvrager onder andere het doel van
het project, de relevantie voor de regeling, de haalbaarheid, een korte versie van
het onderzoeksvoorstel en een globale inschatting van het budget. Daarnaast bevat
het steunbetuigingen van relevante beroepsgroep(en), van relevante patiëntenorganisatie(s)
en, indien aan de orde, van de eigenaar of leverancier van de interventie(s). Dit
ter bevordering van participatie van belanghebbende partijen en (de)implementatie.
Nadat een projectidee is ingediend, zullen de projectideeën getoetst worden door de
commissie. Op verzoek van de commissie zullen bureaumedewerkers van het Zorginstituut
een eerste toets uitvoeren door te bekijken of de interventie-indicatiecombinatie:
-
• geneeskundige zorg, farmaceutische zorg of hulpmiddelen zorg betreft in de zin van
de Zvw en dat de enige reden is waarom de zorg (nog) niet in het basispakket zit,
gelegen is in het feit dat de zorg (nog) niet voldoen aan de ‘de stand van de wetenschap
en praktijk’;
-
• al voldoet aan ‘de stand van de wetenschap en praktijk’, maar vanwege andere redenen
(bv. doelmatigheid) niet uit het basispakket wordt vergoed.
De projectideeën die voldoen aan bovenstaande criteria worden door de commissie getoetst
aan de hand van de overige criteria zoals vermeld in de regeling (inclusief de relevantie
en globaal de kwaliteit). De commissie brengt in beginsel binnen vier maanden na het
indienen van het projectidee advies uit aan de aanvrager over het projectidee om wel
of niet een uitgewerkte subsidieaanvraag in te dienen, met een toelichting daarop.
Bij een advies om een uitgewerkte subsidieaanvragen in te dienen, verwerkt de commissie
in zijn adviesbrief aandachtspunten voor het uitwerken van de aanvraag. Bij een advies
om geen uitgewerkte subsidieaanvragen in te dienen, kan de aanvrager toch een uitgewerkte
subsidieaanvraag indienen. In dat geval wordt de aanvrager dringend verzocht uiterlijk
zes weken na dagtekening van de adviesbrief te melden dat hij toch een uitgewerkte
subsidieaanvraag wil indienen.
Fases 2 en 3. De uitgewerkte subsidieaanvraag
De termijn voor het indienen van een uitgewerkte subsidieaanvraag is in beginsel twee
maanden. De subsidieaanvraag is uitgebreider dan het projectidee en gaat meer in op
de aanpak. Zo dient de subsidieaanvraag ook een systematische review van de effectiviteit
en kosteneffectiviteit te omvatten, een uitgebreidere versie van het onderzoeksvoorstel,
en intentieverklaringen van betrokken centra. Tot slot, moet de aanvrager een begroting
indienen, gebaseerd op de werkelijke kosten van de zorg en het onderzoek, gespecificeerd
naar activiteiten zoals opgenomen in de subsidieaanvraag.
Nadat de aanvraag is ingediend, benadert ZonMw referenten die de aanvragen beoordelen.
Deze referenten beoordelen binnen circa 3 weken de kwaliteit van de aanvragen en brengen
ieder een rapport uit. De kwaliteitsoordelen van de referenten worden (in geanonimiseerde
vorm) aan de aanvragers toegestuurd. De aanvrager wordt vervolgens in de gelegenheid
gesteld om binnen 2 weken een schriftelijke reactie te geven. Op basis van de aanvraag,
referentenrapporten en de reactie van de aanvrager op de rapporten geeft de commissie
advies aan de Raad van Bestuur van het Zorginstituut over subsidieverlening. De commissie
mag gemotiveerd afwijken van het oordeel van de referenten. Hiertoe kan de reactie
van de aanvrager bv. aanleiding geven. Ook kan de commissie de argumenten van een
referent anders wegen of bij verschillen tussen referenten de argumenten van één referent
(bv. de klinische expert) zwaarder meewegen. De commissie adviseert de Raad van Bestuur
van het Zorginstituut over de prioritering aan de hand van de prioriteringsmatrix.
Verder toetst het Zorginstituut de aanvraag aan de hand van de administratieve- en
uitvoeringscriteria (incl. checken budget op realiteitsgehalte), zodat de subsidieverlening
in overeenstemming met de toepasselijke wet- en regelgeving rechtmatig kan worden
uitgevoerd. Indien gewenst door het Zorginstituut, dient de eigenaar of leverancier
een volledig en recent overzicht van zijn financiële situatie te overleggen. Het Zorginstituut
stuurt in beginsel binnen vijf maanden na het indienen van de uitgewerkte subsidieaanvraag
een beschikking of brief aan de aanvrager met daarin het gemotiveerde besluit dat
de subsidieaanvraag is gehonoreerd of afgewezen.
Gevolgen
Met het inzetten van de subsidieregeling worden door VWS de volgende effecten beoogd:
-
a) de subsidieregeling stimuleert dat interventies waarbij enkel nog de (kosten)effectiviteit
dient te worden aangetoond sneller doorstromen naar het basispakket en daarmee eerder
toegankelijk zijn voor de patiënt
-
b) meer effectieve aanwending van de structureel voor de subsidieregeling gereserveerde
middelen
-
c) zorgaanbieders beter inzicht krijgen in de (kosten)effectiviteit van veelbelovende
zorg
-
d) de subsidieregeling aantrekkelijker en beter toegankelijk wordt voor MKB’s, start-ups
en reguliere ziekenhuizen dan het instrument voor voorwaardelijke toelating.
Gevolgen voor regeldruk en administratieve lasten
In de uitvoeringstoets van het Zorginstituut is in een impactanalyse bezien welke
gevolgen de subsidieregeling heeft voor de administratieve processen van de bij de
regeling betrokken partijen. De verwachting is dat de regeling ten opzichte van het
instrument voorwaardelijke toelating een verlaging van de lastendruk betekent. Het
doel van de herinrichting van de regeling is immers het verlagen van de administratieve
lastendruk en vereenvoudigen en verkorten van de procedure voor partijen, zodat deze
aantrekkelijker wordt. Zo is de verplichting van de voorwaardelijke toelating van
een (vaak langdurige) convenantsfase komen te vervallen, die nodig was om tot juridische
waarborgen van het breed toegankelijke onderzoek te komen. Tevens hebben zorgverzekeraars
geen rol meer in de uitvoering van de voorwaardelijke toelatingstrajecten, wat ook
een aanzienlijke vermindering van administratieve complexiteit met zich meebrengt.
Uitvoering
De subsidieregeling wordt in mandaat uitgevoerd door het Zorginstituut, in samenwerking
met ZonMw. Expertise van beide organisaties is nodig voor goede uitvoering van de
regeling. Het mandaat voor de uitvoering van de subsidieregeling ligt bij het Zorginstituut.
Besluitvorming over de subsidieregeling ligt derhalve bij het Zorginstituut.
De uitvoeringsconsequenties, specificering van de werkzaamheden en benodigde capaciteit
zijn door beide uitvoerende partijen uitgewerkt in de uitvoeringstoets van september
2018.
Partijen die bij de subsidieregeling zijn betrokken, zijn:
-
a) indiener: de indiener is verantwoordelijk voor de tijdig aanbieding van een projectidee
en later een uitgewerkte aanvraag bij het Zorginstituut.
-
b) beroepsgroep en patiëntenorganisatie: De beroepsgroep en patiëntenvereniging dienen
betrokken te zijn bij het opstellen en de uitvoer van het project en dienen aanvragen
van een steunbetuiging te voorzien.
-
c) eigenaar of leverancier van de interventie: deze partijen worden aangemoedigd om deel
te nemen aan de projecten en dienen aanvragen van een steunbetuiging te voorzien.
-
d) Zorginstituut Nederland: Het Zorginstituut brengt haar expertise en ervaring in omtrent
pakketbeheer; de beoordeling of het onderzoeksvoorstel de pakketvraag beantwoord en
de uiteindelijke beoordeling of de data van het onderzoek genoeg vertrouwen geven
in de (kosten)effectiviteit van de interventie om deze op te nemen in het basispakket.
-
e) ZonMw: ZonMw brengt haar expertise en ervaring in omtrent het programmeren van praktijkgericht
onderzoek via subsidieregelingen, inclusief het beoordelen en monitoren van de kwaliteit
van wetenschappelijke onderzoeksvoorstellen.
Financiële gevolgen
Structureel wordt jaarlijks circa € 70 miljoen beschikbaar gesteld voor de financiering
van gehonoreerde onderzoeken. Voor de uitvoering van de regeling door het Zorginstituut
Nederland en ZonMw is jaarlijks vanaf 2019 circa € 1.050.000 benodigd, oplopend tot
circa € 1.240.000 in 2023.
Evaluatie
De subsidieregeling wordt na één jaar geëvalueerd. Daarnaast stelt het Zorginstituut
jaarlijks een inhoudelijk verslag op over de stand van zaken over alle projectideeën,
potentiële projecten en eventuele knelpunten die zich voordoen bij de (uitvoering
van de) regeling. Door de vormgeving via het subsidie-instrument is de regeling flexibel
aanpasbaar. Op het moment dat blijkt dat bepaalde aspecten niet optimaal werken is
de flexibiliteit aanwezig om de regeling op onderdelen aan te passen.
Advies en consultatie
De plannen voor de nieuwe regeling zijn in het voorjaar van 2018 in diverse bijeenkomsten
besproken met een brede groep van (toekomstige) gebruikers. Deze partijen hebben aangegeven
dat de regeling aan de belangrijkste knelpunten van de huidige regeling voor voorwaardelijke
toelating tegemoet komt. Partijen waren onder meer zeer te spreken over de mogelijkheid
voor het indienen van een projectidee, de advisering over de onderzoeksopzet bij de
aanvraag en de snellere doorlooptijd van de procedure. Ook onderschrijven partijen
de keuze om de zorg niet meer breder toegankelijk aan patiënten aan te bieden dan
noodzakelijk is voor het onderzoek.
In de consultatiebijeenkomsten zijn tevens waardevolle suggesties voor de verdere
uitwerking naar voren gebracht. Voorbeelden hiervan zijn de overgenomen suggesties
om 1) aan het begin van de onderzoekstrajecten zoveel mogelijk bij de interventie
betrokken stakeholders aan te laten sluiten 2) de criteria zo transparant mogelijk
te publiceren en 3) de nieuwe subsidieregeling na één jaar te evalueren. Partijen
geven aan te verwachten dat de regeling een stimulans geeft om potentieel veelbelovende
zorg sneller bij de patiënt te krijgen.
Inwerkingtreding
De subsidieregeling treedt per 1 februari 2019 in werking.
Artikelsgewijs
Artikel 1.1
In dit artikel zijn de begripsbepalingen opgenomen. Twee belangrijke begrippen zijn
het kwaliteitsoordeel en het relevantieoordeel van de commissie. De commissie adviseert
het Zorginstituut op basis van haar oordeel over de kwaliteit van het onderzoek en
haar oordeel over de relevantie van de interventie-indicatiecombinatie.
De kwaliteit van het onderzoek blijkt uit vraagstelling, hypothese, plan van aanpak,
haalbaarheid, expertise projectgroep en systematische review. Ter toelichting op die
aspecten wordt het volgende opgemerkt. De vraagstelling bevat de concrete en toetsbare
onderzoeksvraag/vragen. De hypothese bevat het verwachte antwoord op de vraagstelling.
De onderzoeksopzet bevat de uit te voeren stappen (inclusief PICOTs: Patient Intervention
Comparison Outcome Time study design) voor het bepalen van de effectiviteit van de
interventie-indicatiecombinatie ten opzichte van de standaard- of gebruikelijke behandeling
in Nederland met een onderbouwing voor de keuzes, of – indien er geen alternatieve
behandeling is bij de indicatie – een vergelijking van de interventie met ‘best ondersteunende
zorg’ of ‘niets doen’. De onderzoeksopzet dient zodanig te zijn dat de hypothese getoetst
en eventueel verworpen kan worden. De uitkomstmaten bevatten de primaire en secundaire
uitkomstmaten waarmee de relatieve effectiviteit wordt beoordeeld en een onderbouwing
voor de keuzes. De formulering van de primaire uitkomstmaat is op patiëntniveau (mortaliteit
/ morbiditeit / kwaliteit van leven / complicaties). De data-analyse bevat de voorgenomen
analyses van de onderzoeksgegevens en een onderbouwing voor de keuzes. De samplesizeberekening
bevat de berekening van de benodigde steekproefgrootte en een onderbouwing voor de
keuzes. De berekening is gebaseerd op eigen vooronderzoek of de systematische review
die de aanvrager bij de aanvraag indient. De economische evaluatie bevat de uit te
voeren stappen voor het bepalen van de kosteneffectiviteit en budget impact analyse
van de interventie-indicatiecombinatie ten opzichte van de standaard- of gebruikelijke
behandeling in Nederland en een onderbouwing voor de keuzes. De haalbaarheid bevat
de onderbouwing dat het onderzoek haalbaar is binnen de gevraagde subsidielooptijd,
waarbij ingegaan wordt op belemmeringen en risicofactoren voor de inclusie. Voor meer
informatie over potentiële belemmeringen en risicofactoren met betrekking tot de inclusie
kan de aanvrager de publicatie “succesvol includeren” van ZonMw betrekken. Uit de
beschrijving van de expertise van de onderzoeksgroep wordt duidelijk welke projectdeelnemers
over de benodigde expertise beschikken voor het slagen van het onderzoek en voor de
(de)implementatie. De systematische review bevat een systematisch overzicht van de
relevante gepubliceerde studies.
De relevantie van een interventie blijkt uit de verwachte effectiviteit en de kosten
in vergelijking met standaard- of gebruikelijke behandeling(en) in Nederland en de
ziektelast van de indicatie. Hierbij kan de commissie gebruik maken van de referentiewaarde
voor de maximale meerkosten zoals beschreven in het rapport ‘Kosteneffectiviteit in
de praktijk’ van het Zorginstituut (2015, p.21).
Met ATMP’s worden medicinale producten gebaseerd op genen, cellen of weefsels bedoeld,
die vooral worden ingezet ten behoeve van onder meer behandeling van genetische afwijkingen,
regeneratieve geneeskunde, immunotherapie van kanker en (auto-)immuunziekten.
Artikel 1.2
Hoofdstuk 5 van de Kaderregeling subsidies OCW, SZW en VWS is van toepassing. In dit
hoofdstuk staan verplichtingen voor de subsidieontvanger beschreven.
Artikel 1.3
Subsidie wordt uitsluitend verstrekt indien de hoofdaanvrager met de Staat een overeenkomst
sluit waarbij de Staat hem belast met en hij zich verplicht tot het verrichten van
de hiervoor omschreven dienst van algemeen economisch belang (DAEB). De DAEB die gevestigd
wordt heeft betrekking op de zorg en het daarvoor benodigde onderzoek. De met het
onderzoek opgedane kennis zal om niet aan een ieder ter beschikking moeten worden gesteld, in ieder geval door middel van
publicaties. Het Zorginstituut sluit namens de Staat de DAEB-overeenkomst met de aanvrager.
Artikel 1.4
Uitgangspunt van de Zorgverzekeringswet is dat alleen zorg die voldoet aan ‘de stand
van de wetenschap en praktijk’ tot het basispakket behoort. Op grond van deze regeling
is subsidie mogelijk voor onderzoek over de effectiviteit en kosteneffectiviteit van
de interventie die nog niet tot het basispakket behoort. Deze mogelijkheid geldt alleen
voor geneeskundige zorg (inclusief diagnostica), hulpmiddelen, off-label geneesmiddelen
en ATMPs die niet voldoen aan het criterium ‘de stand van de wetenschap en praktijk’
en uitsluitend om die reden geen deel uitmaken van het basispakket. Een interventie
die vanwege andere wettelijke beperkingen niet voor vergoeding vanuit het basispakket
in aanmerking komt, komt niet in aanmerking voor subsidie. Kortdurende fysiotherapie
en cosmetische chirurgie zijn voorbeelden van zorg die vanwege wettelijke beperkingen
zijn uitgesloten van de basisverzekering.
De aanvrager kan via de regeling financiering aanvragen voor zowel de kosten van de
interventie als de onderzoekskosten die tijdens het onderzoek worden gemaakt. Maximaal
20% van de totale budget mag aan onderzoek besteed worden. Indien de onderzoekskosten
meer dan 20% van het totale budget bedragen, dan dient te worden onderbouwd dat de
additionele kosten (boven de 20%) uit private middelen kunnen worden bekostigd.
Artikel 1.5
In dit artikel is een aantal uitsluitingsbepalingen opgenomen.
Indien de belemmering voor de uitvoering van het onderzoek alleen in de onderzoekskosten
ligt, zijn er andere subsidiemogelijkheden voor een onderzoek, bijvoorbeeld bij ZonMw.
Vanwege een doelmatige besteding van het maximaal beschikbare budget voor subsidieverlening
komt onderzoek naar de off-label toepassing van een geneesmiddel waarvoor de marktautorisatie
minder dan 7 jaar geleden is verstrekt niet in aanmerking voor subsidiëring. Bepalend
voor die termijn zal de indieningsdatum van de aanvraag zijn. Om diezelfde reden is
onderzoek naar de off-label toepassing bij een indicatie die in Nederland vaker voorkomt
dan 1 op de 150.000 inwoners uitgesloten van subsidiëring.
Daarnaast mag het onderzoek geen doublure zijn van eerder, startend of lopend onderzoek,
tenzij onderbouwd wordt dat de resultaten van aanvullend onderzoek noodzakelijk zijn
voor de beoordeling van ‘de stand van de wetenschap en praktijk’. Ook deelname van
Nederlandse centrum/centra aan onderzoek dat bij indiening van aanvraag al gestart
is, komt niet in aanmerking voor subsidie. Tot slot, de maximale termijn voor verstrekking
van de subsidie is zes jaar. Projecten die volgens de aanvraag langer dan zes jaren
gaan duren, komen evenmin voor subsidie in aanmerking.
Artikel 1.6
Voor geneesmiddelen geldt dat marktregistratie in de regel voldoende is om de veiligheid
aan te tonen. Voor medische technologie, met name devices en protheses, geldt dat
een CE-keurmerk niet per definitie voldoende is om de veiligheid aan te tonen en de
werkzaamheid aannemelijk te maken.
Voor de start van het onderzoek is een positief oordeel van een METC of een niet-Wet
medisch-wetenschappelijk onderzoek (WMO) verklaring noodzakelijk.
Artikel 1.7
Voor het begrip verzekerden wordt verwezen naar artikel 1, onderdeel f, van de Zorgverzekeringswet.
Voor de toepassing van de Subsidieregeling worden gemoedsbezwaarden en verdragsgerechtigden
gelijkgesteld aan verzekerden. Gemoedsbezwaarden zijn op dezelfde wijze gedefinieerd
als in artikel 2, tweede lid, onderdeel b, van de Zorgverzekeringswet. Verdragsgerechtigden
zijn in algemene zin omschreven. Meer concreet gaat het om personen die op grond van
Verordening (EU) nr. 883/2004 betreffende de coördinatie van socialezekerheidsstelsels
recht hebben op zorg alsof zij krachtens een zorgverzekering verzekerd zijn. Daarnaast
heeft Nederland met diverse andere landen verdragen afgesloten waarin vergelijkbare
rechten zijn toegekend.
Artikel 1.8
Het onderzoek moet gegevens van ten minste voldoende kwaliteit opleveren zodat het
Zorginstituut op basis van deze gegevens kan beoordelen of de interventie-indicatiecombinatie
voldoet aan ‘de stand van de wetenschap en praktijk’. In het rapport van het Zorginstituut
uit 2015 ‘Beoordeling stand van de wetenschap en praktijk’ staat beschreven hoe het
Zorginstituut dit beoordeeld.
Verder moet het onderzoek gegevens van ten minste voldoende kwaliteit opleveren zodat
het Zorginstituut de kosteneffectiviteit en de landelijke budget impact van de interventie-indicatiecombinatie
kan beoordelen. Het berekenen van de kosteneffectiviteit en de budgetimpact staat
beschreven in de ‘Richtlijn voor het uitvoeren van economische evaluaties in de gezondheidszorg’
van het Zorginstituut uit 2016. Bij de kosteneffectiviteitsanalyse dienen de kosten
te worden gekwantificeerd vanuit twee perspectieven: het maatschappelijk perspectief
en het gezondheidszorgperspectief.
Artikel 1.9
Met dit artikel wordt voorkomen dat aanvragen worden gehonoreerd waarvan de kwaliteit
van het onderzoek niet voldoende is of waarvan de relevantie van de interventie-indicatiecombinatie
te laag is.
Artikel 1.10
Voor de subsidieverlening geldt een subsidieplafond. Voor de eerste ronde is een afzonderlijk
bedrag bepaald. Mocht het plafond voor de eerste ronde niet bereikt worden, dan kan
het resterende bedrag in de tweede ronde worden toegekend, tot aan het plafond voor
het gehele jaar. Indien met de toekenning van de uitgewerkte aanvragen die aan alle
criteria voldoen het bedrag van het subsidieplafond in een ronde zou worden overschreden,
dan wordt het beschikbare budget verdeeld op basis van rangorde. De rangorde wordt
bepaald met de prioriteringsmatrix, zoals opgenomen bij artikel 2.6. Indien twee of
meer aanvragen een gelijke rangorde hebben op de grens van het subsidieplafond, dan
wordt er – onder toezicht van een notaris – geloot tussen deze aanvragen.
Hoofdstuk 2. De aanvraagprocedure
Artikel 2.1, 2.2, 2.3 en 2.4
Voor het indienen van de projectideeën en aanvragen maakt het Zorginstituut gebruik
van het indieningssysteem van ZonMw. De uiterste indieningsdatum voor de projectideeën
en de aanvragen wordt in ieder geval op de website van het Zorginstituut gepubliceerd.
Om er voor te zorgen dat de projectideeën en de aanvragen alle elementen bevatten
die belangrijk zijn voor de beoordeling wordt een door de minister vastgesteld formulier
gebruikt. Dit formulier kan worden ingevuld via het indieningssysteem van ZonMw.
Artikel 2.2, onderdeel e: aannemelijk maken marktfalen
Het is aan de subsidieaanvrager om aannemelijk te maken dat er sprake is van marktfalen.
Om te kunnen beoordelen of de aanvrager aannemelijk heeft gemaakt dat sprake is van
marktfalen zal de aanvrager onder meer inzichtelijk moeten maken wat de verwachte
onderzoekskosten zijn en wat de verwachte zorgkosten zijn – en waar die verwachting
op gebaseerd is.
De zorgaanbieder zal moeten onderbouwen waarom hij zijn onderzoek en zorgkosten niet
gefinancierd kan krijgen. Als de fabrikant participeert in het onderzoek moet de fabrikant
aantonen dat de te verwachten opbrengsten niet opwegen tegen de kosten van de investeringen.
Er kan sprake zijn van marktfalen als het onderzoek naar veelbelovende zorg dat aan
de criteria uit de regeling voldoet zonder de aangevraagde subsidie niet uitgevoerd
kan worden. De belemmering voor de uitvoering van het onderzoek moet van financiële
aard zijn. Ten minste een deel van de financiële belemmering voor het kunnen uitvoeren
van het onderzoek moet zijn gelegen in de met het onderzoek gepaard gaande zorgkosten.
Onderzoek waarbij de financiële belemmering voor het onderzoek uitsluitend in de onderzoekskosten
van het onderzoek is gelegen, komt niet in aanmerking voor subsidie.
De financiële belemmeringen kunnen om verschillende redenen ontstaan, die ook door
elkaar kunnen lopen. Te denken valt bijvoorbeeld aan:
-
a. de grote omvang van de vereiste investeringen voor het onderzoek (inclusief zorgkosten)
in relatie tot de financiële middelen van de aanvrager. Met andere woorden: de aanvrager
heeft het geld niet en kan daar op de markt ook niet aan komen.
-
b. de omvang van de potentiële markt. Als de interventie-indicatiecombinatie wordt toegelaten
tot het pakket wegen de verwachte opbrengsten voor de fabrikant/eigenaar van de interventie-indicatiecombinatie
niet op tegen de kosten die met het onderzoek gepaard gaan.
-
c. de fabrikant/eigenaar van de interventie-indicatiecombinatie heeft geen belang bij
het onderzoek omdat hij zonder het onderzoek een andere, winstgevende, interventie
kan blijven verkopen. Indien de interventie-indicatiecombinatie wordt toegelaten tot
het pakket leidt dat tot publieke besparingen maar eveneens tot een vermindering van
private winsten.
-
d. de fabrikant/eigenaar van de interventie-indicatiecombinatie heeft geen belang bij
het onderzoek omdat het middel al op andere markten/landen is toegelaten en hij met
het bedienen van die markten de grens van zijn productiecapaciteit heeft bereikt.
-
e. de verwachte financiële opbrengsten voor de fabrikant/eigenaar interventie-indicatiecombinatie
zijn gering, terwijl de verwachte besparing (op termijn) van zorgkosten groot is.
Artikel 2.3
Om de kwaliteit van de aanvragen te verhogen wordt eerst een projectidee ingediend.
Deze projectideeën worden op verzoek van de commissie door bureaumedewerkers van het
Zorginstituut getoetst op enkele formele criteria. Zij bekijken of de interventie-indicatiecombinatie:
-
• geneeskundige zorg, farmaceutische zorg of hulpmiddelen zorg betreft in de zin van
de Zvw en dat de enige reden is waarom de zorg (nog) niet in het basispakket zit,
gelegen is in het feit dat de zorg (nog) niet voldoen aan de ‘de stand van de wetenschap
en praktijk’;
-
• al voldoet aan ‘de stand van de wetenschap en praktijk’, maar vanwege andere redenen
(bv. doelmatigheid) niet uit het basispakket wordt vergoed.
Als niet wordt voldaan aan één van bovenstaande criteria, dan stuurt de commissie
een brief aan de indiener van het projectidee met een niet-bindend advies om geen
aanvraag in te dienen met een toelichting daarop.
De commissie toetst de projectideeën aan de overige criteria van de regeling, waaronder
relevantie en kwaliteit. De commissie brengt in beginsel binnen vier maanden na het
indienen van het projectidee niet-bindend advies uit aan de indieners van het projectidee
om wel of niet een aanvraag in te dienen.
Artikel 2.5, onderdeel f:
Bij het onderzoek dienen bij voorkeur meerdere onderzoekscentra/zorgaanbieders betrokken
te zijn, verspreid over het land. Hierop kan mits voldoende onderbouwd een uitzondering
gemaakt worden.
Artikel 2.5, onderdeel g: beschrijving exit-procedure
Van belang is dat een aanvrager de wijze waarop het onderzoek zorgvuldig kan worden
beëindigd heeft uitgewerkt. De aanvrager geeft daartoe in het aanvraagformulier aan
op welke medisch verantwoorde wijze een niet-éénmalige behandeling, zoals chronisch
gebruik van een geneesmiddel of neurostimulatie wordt beëindigd respectievelijk afgebouwd
zodra de deelname van een patiënt aan het onderzoek (vroegtijdig) is gestopt. Hierbij
wordt vastgelegd welke partijen de kosten van medisch verantwoorde afbouw of continuering
van de behandeling voor hun rekening nemen totdat het standpunt van het Zorginstituut
over de pakketwaardigheid van de interventie-indicatiecombinatie gepubliceerd is.
Artikel 2.6
Voor een zorgvuldige inhoudelijke beoordeling van de aanvraag wordt de aanvraag eerst
voorgelegd aan referenten. Deze referenten beoordelen op verzoek van ZonMw de aanvraag
op de in de regeling genoemde kwaliteitsaspecten.
Artikel 2.7
In dit artikel is de prioriteringsmatrix opgenomen voor de prioritering van de aanvragen.
De rangorde wordt bepaald op basis van het commissieoordeel over kwaliteit en relevantie.
Voor kwaliteit wordt gewerkt met een vijfpuntschaal en voor relevantie met een driepuntschaal.
De commissie brengt haar advies over de prioritering uit aan de Raad van Bestuur van
het Zorginstituut.
Artikel 3.1
Het Zorginstituut besluit in beginsel binnen vijf maanden na het indienen van de aanvraag
op de aanvraag. Hij geeft daarin gemotiveerd aan waarom de aanvraag is gehonoreerd
of afgewezen.
Artikel 3.2
De looptijd voor een project is maximaal zes jaar en dient goed onderbouwd te worden.
De aanvrager dient hierbij onder andere te onderbouwen waarom hij van mening is dat
de resultaten van het onderzoek niet verouderd zijn op het moment dat het onderzoek
wordt afgerond. Dat is bijvoorbeeld het geval als in Nederland de standaard- of gebruikelijke
behandeling tijdens het project verandert.
Voor een subsidieontvanger van een lopend project bestaat de mogelijkheid om een verzoek
om een (budgetneutrale) verlenging in te dienen bij het Zorginstituut waarmee de projectduur
verlengt kan worden tot maximaal zeven jaar. Dit verzoek toetst het Zorginstituut
aan de hand van de administratieve- en uitvoeringscriteria. Bovendien moet aannemelijk
zijn gemaakt dat het Zorginstituut aan het einde van het traject kan beoordelen of
de interventie-indicatiecombinatie voldoet aan ‘de stand van de wetenschap en praktijk’.
Artikel 4.1
Naast de verplichtingen uit de Algemene wet bestuursrecht en hoofdstuk 5 van de Kaderegeling
subsidies OCW, SZW en VWS zijn in artikel 4.1. en 4.2 enkele aanvullende verplichtingen
voor subsidieontvangers opgenomen.
Een subsidieontvanger moet er voor zorgen dat hij de METC-goedkeuring binnen 12 maanden
na de subsidieverlening heeft ontvangen. Indien geen goedkeuring binnen 12 maanden
is ontvangen, kan het Zorginstituut de subsidieverlening intrekken of wijzigen. In
de verleningsbeschikking kan worden opgenomen dat de subsidieontvanger vooruitlopend
op de METC-goedkeuring met het project mag starten. Na een positief oordeel van een
METC, of een niet-WMO verklaring, start het onderzoek met als doel het verzamelen
van gegevens over de effectiviteit en kosteneffectiviteit van de interventie-indicatiecombinatie.
Om te voorkomen dat er geen, te traag of onderzoeksgegevens van onvoldoende kwaliteit
worden verzameld, is het noodzakelijk dat de voortgang van de onderzoekstrajecten
gevolgd worden. Dit zullen ZonMw en het Zorginstituut enerzijds doen via (in beginsel)
jaarlijkse klankbordbijeenkomsten en anderzijds via jaarlijkse voortgangsverslagen.
Het is de taak van de subsidieontvanger om de klankbordbijeenkomsten te organiseren.
De subsidieontvanger dient elke wijziging in projectaanpak te melden bij het Zorginstituut.
ZonMw en het Zorginstituut kunnen de gezamenlijke commissie om advies vragen over
lopende projecten, bijvoorbeeld als het onderzoek traag verloopt of als de subsidieontvanger
een wijziging wil aanbrengen in de activiteiten waarvoor subsidie is verleend. Het
Zorginstituut kan de subsidieverlening intrekken of ten nadele van de subsidieontvanger
wijzigen, indien de activiteiten waarvoor subsidie is verleend niet of niet geheel
hebben plaatsgevonden of zullen plaatsvinden. Te denken valt dan aan een zodanige
verandering van de standaard- of gebruikelijke behandeling tijdens de onderzoeksduur,
dat daardoor de pakketwaardigheid van de interventie-indicatiecombinatie niet meer
beoordeeld kan worden of aan een vertraging van het onderzoek waardoor dat hoogstwaarschijnlijk
niet binnen de maximale projecttermijn van zeven jaar kan worden afgerond.
Met publiek geld gefinancierde resultaten van projecten dienen publiekelijk beschikbaar
te zijn voor delen en hergebruik, in het bijzonder voor nieuw wetenschappelijk onderzoek.
Daarom is in artikel 4.1, onder d, de verplichting opgenomen dat de subsidieontvanger
ervoor moet zorgen dat publicaties die uit het project voortkomen direct en vrij toegankelijk
zijn via een ‘Open Access’. Er is een verbod op geheimhouding van kennis voortkomend
uit de projecten, tenzij er zwaarwegende belangen zijn (privacy, octrooiaanvraag)
die tijdelijk geheimhouding noodzakelijk maken. Indien een subsidieontvanger in verband
met een octrooiaanvraag de publicatie van kennis tijdelijk wil opschorten, kan hij
daartoe een verzoek indienen bij het Zorginstituut. Daarnaast is in artikel 4.1 onder
e, de verplichting opgenomen om uit het project voortkomende databestanden beschikbaar
te stellen volgens de principes van FAIR data.
Artikel 4.2
Het is van belang dat het Zorginstituut zo snel mogelijk na afloop van het project
over het eindverslag beschikt zodat zo snel mogelijk beslist kan worden over toelating
van de indicatie-interventiecombinatie.
Het liefst binnen één week, maar in elk geval binnen een maand na afloop van het project
dient de subsidieontvanger een inhoudelijk eindverslag in. Het inhoudelijk eindverslag
dient in ieder geval de genoemde documenten te bevatten. Daarnaast kunnen de volgende
documenten onderdeel uitmaken van het eindverslag:
-
• Bij additionele publicatie(s), naast het manuscript van de subsidieontvanger: een
systematische review over de effectiviteit van de interventie-indicatiecombinatie,
waarin de recente internationale literatuur en de resultaten van het onderzoek van
de subsidieontvanger zijn verwerkt.
-
• Bij additionele publicatie(s): een systematische review over de kosteneffectiviteit
van de interventie-indicatiecombinatie, waarin de recente internationale literatuur
en de resultaten van het onderzoek van de subsidieontvanger zijn verwerkt.
Artikel 5.1
In beginsel worden de voorschotten jaarlijks verstrekt. Bij de beslissing tot subsidieverlening
wordt een schema vastgesteld tot bevoorschotting tot maximaal 90% van het totale subsidiebedrag.
Het Zorginstituut verstrekt de voorschotten in overeenstemming met het vastgestelde
bevoorschottingsschema. Bij wijzigingen of vertragingen in het project kan het Zorginstituut
besluiten de bevoorschotting aan te passen.
Artikel 6.1
Voor de vaststelling van de subsidie dient de subsidieontvanger een activiteitenverslag
in waarvan de inrichting overeenkomt met het uitgewerkte onderzoeksvoorstel uit de
aanvraag tot subsidieverlening. Aan de hand van dat verslag kan het Zorginstituut
beoordelen of de activiteiten waarvoor subsidie is verleend daadwerkelijk hebben plaatsgevonden.
Daarnaast dient de subsidieontvanger een financieel eindverslag in dat aansluit bij
de begroting en waaruit de werkelijke kosten van het project blijken, voorzien van
een controleverklaring. Dit financieel verslag is eveneens van belang in verband met
de gevestigde DAEB.
Daarnaast dient de subsidieontvanger een rapport van feitelijke bevindingen in omtrent
de naleving van de overige aan de subsidie verbonden verplichtingen.
Zowel de controleverklaring als het rapport van feitelijke bevindingen zijn opgesteld
door een accountant.
De Minister voor Medische Zorg,
B.J. Bruins