Kamerstuk
| Datum publicatie | Organisatie | Vergaderjaar | Dossier- en ondernummer |
|---|---|---|---|
| Tweede Kamer der Staten-Generaal | 2020-2021 | 25295 nr. 745 |
Zoals vergunningen, bouwplannen en lokale regelgeving.
Adressen en contactpersonen van overheidsorganisaties.
U bent hier:

| Datum publicatie | Organisatie | Vergaderjaar | Dossier- en ondernummer |
|---|---|---|---|
| Tweede Kamer der Staten-Generaal | 2020-2021 | 25295 nr. 745 |
Aan de Voorzitter van de Tweede Kamer der Staten-Generaal
Den Haag, 20 november 2020
Een goed werkend vaccin is de belangrijkste troef om de wereldwijde verspreiding van het coronavirus een halt toe te roepen. We zijn uiteindelijk pas beschermd als er werkende vaccins zijn. Daarom werken onderzoekers wereldwijd aan meer dan 200 vaccins tegen het coronavirus. De ontwikkelingen zijn bemoedigend; momenteel bevinden tientallen kandidaat-vaccins zich in de laatste fase van het klinische onderzoek. Nederland heeft nu, via de Europese Commissie, afspraken gemaakt met zes verschillende vaccinontwikkelaars. Vanzelfsprekend kunnen we pas over een vaccin beschikken als alle testfases goed doorlopen zijn en het Europees Medicijnagentschap (EMA) heeft aangegeven dat het vaccin effectief en veilig is – want dat is een absolute voorwaarde.
In mijn brief van 23 september jl.1 heb ik uw Kamer geïnformeerd over de stappen die het kabinet in de afgelopen maanden heeft gezet om snel te kunnen starten met vaccineren. Deze stappen werk ik hierbij verder uit, inclusief het eerste besluit van het kabinet in relatie tot de vaccinatiestrategie en de daarbij horende prioritering. Met deze brief geef ik tevens invulling aan de motie van het lid Pieter Heerma c.s. over een uitvoeringsstrategie voor het vaccineren van de Nederlandse samenleving.2 Daarbij wil ik benadrukken dat het proces rondom de COVID-19 vaccinatie nog onbekendheden bevat. We weten nog niet welke vaccins uiteindelijk tot de markt zullen worden toegelaten, op welk moment dat gebeurt, en in welke hoeveelheden. Ook weten we niet voor welke groepen deze vaccins geschikt zullen zijn. Het kabinet bereidt zich daarom – samen met verschillende partijen – voor op meerdere scenario’s, en zal de strategie herzien op het moment dat de beschikbare informatie daarom vraagt. Op basis van de meest recente informatie verwacht ik dat begin 2021 gestart kan worden met de eerste vaccinaties. Vanzelfsprekend zal ik uw Kamer op de hoogte houden van ontwikkelingen.
Om de uitvoering van de vaccinatie te bespoedigen, heeft het kabinet parallel aan het adviestraject van de Gezondheidsraad aan het RIVM gevraagd de voorbereiding van de vaccinatiecampagne ter hand te nemen en een verkenning te doen onder mogelijke uitvoerende partijen. Samen met diverse internationale rapporten3 vormen deze twee adviezen het vertrekpunt voor de Nederlandse vaccinatiestrategie. Hiertoe hebben we met het RIVM en andere partijen verschillende elementen verder uitgewerkt, zoals de logistieke voorbereidingen en veiligheidsaspecten, de selectie van doelgroepen, de uitvoering, de planning en de communicatie.
Leeswijzer
In deze vaccinatiestrategie ga ik allereerst in op enkele algemene punten (paragraaf 1), de aankoopstrategie rond de COVID-19 vaccins (paragraaf 2) en de veiligheid, toelating en leveringstermijnen (paragraaf 3). Vervolgens benoem ik in paragraaf 4 de hoofdpunten uit het advies van de Gezondheidsraad, dat ik op 19 november jl. naar uw Kamer heb gestuurd. De kabinetsreactie op dit advies volgt in paragraaf 5. Dan volgt informatie over het oproepen van doelgroepen en de registratie van de COVID-19 vaccinatie (paragraaf 6) de uitvoeringsaspecten van de COVID-19 vaccinatie (paragraaf 7). Tot slot ga ik in op de logistiek (paragraaf 8), de communicatiestrategie (paragraaf 9), monitoring en onderzoek (paragraaf 10), en financiën (paragraaf 11).
Naar aanleiding van vragen van uw Kamer wil ik nogmaals bevestigen dat de COVID-19 vaccinatie niet verplicht wordt. Dit heb ik ook in het debat op 18 november jl. benadrukt. Ik vind echter wel dat mensen een verantwoordelijkheid hebben naar zichzelf, naasten, en andere, meer kwetsbare mensen. Ik zal het belang van vaccineren dan ook blijven benadrukken, waarbij geen sprake zal zijn van een (indirecte) verplichting. Dwang en drang kunnen het draagvlak voor vaccinatie ondermijnen.
Naarmate het aantal mensen dat gevaccineerd is toeneemt, kunnen we voor de vraag komen te staan welke maatregelen nog passend zijn en in welke situaties. Een voorbeeld is de verpleeghuizen. Als in een bepaald verpleeghuis op een gegeven moment alle bewoners en het personeel gevaccineerd zijn, dan kan het zo zijn dat bijvoorbeeld de anderhalve meter niet meer noodzakelijk is. Dit is een vraagstuk dat we, aan de hand van de dan geldende situatie, steeds opnieuw tegen het licht moeten houden.
Het lid Segers (CU) heeft tijdens het debat van 18 november jl. (Handelingen II 2020/21, nr. 26, Debat over de ontwikkeling rondom het coronavirus) een motie ingediend waarin hij het kabinet vraagt zich te laten adviseren door een gezaghebbend instituut over een ethisch afwegingskader voor de vaccinatiestrategie4. Het gaat daarbij met name om de spanning tussen het collectief belang en de individuele vrijheid. Op de verdere uitwerking zal ik na de stemming over de motie in de volgende voortgangsbrief ingaan. Hierbij betrek ik ook de ethische afwegingen die de Gezondheidsraad heeft gemaakt in zijn advies over de COVID-19 vaccinatie.
Al sinds het voorjaar werkt het kabinet aan het zo snel mogelijk beschikbaar krijgen van veilige, werkzame en betrouwbare COVID-19 vaccins. Nederland heeft hierbij een leidende rol op zich genomen door samen met Duitsland, Frankrijk en Italië een eerste deal te sluiten met een vaccinproducent. Daarna is deze samenwerking uitgebreid tot een Joint Negotiation Team (JNT) onder leiding van de Europese Commissie. Hierover heb ik u eerder per brief geïnformeerd.
Het doel van dit JNT is het samenstellen van een breed portfolio van kandidaat-vaccins, gebaseerd op verschillende technologieën. Op deze manier doen we er alles aan om de kans op uiteindelijke beschikbaarheid van een vaccin te vergroten.
De onderhandelingen met vaccinontwikkelaars bevinden zich inmiddels in een vergevorderde fase. Met zes producenten zijn afspraken gemaakt over de aanschaf van vaccins voor de Europese landen, waarbij nu met vijf producenten de onderliggende contracten zijn ondertekend. Wanneer de vaccins van al deze producenten succesvol blijken te zijn en markttoelating voor wordt verleend, kan dit voor Nederland leiden tot de beschikbaarheid van circa 50 miljoen vaccins. Hierbij moet worden aangetekend dat bij de meeste kandidaat-vaccins meer dan een dosis nodig is voor effectieve bescherming.
Bij de samenstelling van het portfolio zijn de volgende criteria gehanteerd:
1) Wetenschappelijke kwaliteit van een kandidaat-vaccin: wetenschappelijke experts uit de landen die in het JNT zijn vertegenwoordigd, moeten het eens zijn over de potentie van een kandidaat-vaccin. In dit kader is het kabinet ondersteund door een wetenschappelijk adviespanel, geleid door het RIVM;
2) De tijdige beschikbaarheid van een kandidaat-vaccin tijdens de pandemische fase: het gaat nadrukkelijk om het vroegtijdig beschikbaar krijgen van grote hoeveelheden vaccins in 2020 en 2021;
3) De prijs van een kandidaat-vaccin;
4) Productie in de Europese Unie: de EU onderhandelt met voorrang met partijen die het vaccin in de EU produceren en daar hun capaciteit willen opschalen.
5) De wens om kandidaat-vaccins gebaseerd op uiteenlopende technologieën in portefeuille te hebben, ten einde de kans op een werkend vaccin zo groot mogelijk te maken;
6) De betrouwbaarheid van de producent om vaccins te kunnen produceren en hun mogelijkheden om de productie (in de EU) in korte tijd te kunnen opschalen tot honderden miljoenen vaccins. De producent moet bovendien geacht worden de benodigde hoeveelheden doses onder de wettelijk voorgeschreven wijze te kunnen produceren.
Om die reden heeft de Europese Commissie in haar strategie vastgelegd in de onderhandelingen prioriteit te zullen geven aan het sluiten van contracten met producenten die:
• Reeds in 2020 begonnen zijn met klinische tests;
• Over de expertise en capaciteit beschikken om een succesvol vaccin te ontwikkelen;
• Bewezen capaciteit hebben om al in 2021 hoge volumes te produceren.
Wereldwijde beschikbaarheid vaccins
Ten slotte heeft de Europese Unie de intentie uitgesproken om nadrukkelijk ook bij te dragen aan de beschikbaarheid van vaccins in landen die zelf niet in staat zijn om te voorzien in de behoefte aan vaccins. Hiertoe wordt nauw samengewerkt met de mondiale COVAX-faciliteit. De Europese Unie heeft nu reeds € 500 miljoen aan COVAX beschikbaar gesteld. Nederland heeft – naast een directe bijdrage van € 5 mln. aan COVAX – € 25 miljoen gereserveerd voor de beschikbaarheid van kandidaat-vaccins voor kwetsbare landen. De Europese Commissie en de lidstaten zijn hiermee de grootste donor van de COVAX-faciliteit. Op dit moment wordt nog overlegd hoe de bijdrage van Nederland aan COVAX het best vorm kan worden gegeven (in kind/in cash). Ook heeft Nederland eerder, met een bijdrage van ruim € 500 miljoen, significant bijgedragen aan de ondersteuning van landen die zelf onvoldoende middelen hadden om de pandemie het hoofd te bieden.
Nederland heeft zich vanaf het begin ingezet voor het uitgangspunt dat de EU meer vaccins moet kopen dan voor de eigen bevolking nodig is. Op deze manier willen we met de Europese inkoopkracht bijdragen aan de beschikbaarheid van vaccins in andere delen van de wereld. Binnen de EU werkt Nederland aan een voorstel hoe vaccin-donatie het best kan worden georganiseerd. Binnenkort zal het kabinet hierover een nadere brief aan uw Kamer doen toekomen.
Het beschikbaar komen van vaccins is afhankelijk van het succesvol doorlopen van alle klinische testfasen en de daaropvolgende beoordeling door de Europese medicijnautoriteit (EMA) en het College ter Beoordeling van geneesmiddelen (CBG). Daarnaast speelt ook de productiecapaciteit een rol. De EMA en het CBG hanteren zeer strenge criteria, die hetzelfde zijn als bij het toelaten van vaccins tegen andere infectieziekten. Er worden absoluut geen concessies gedaan aan de beoordeling van de kwaliteit, veiligheid en effectiviteit van het vaccin. Meer informatie over het beoordelingsproces is te vinden op de website van het CBG.5
Vanwege de grote urgentie maken de medicijnautoriteiten nu meer snelheid met de beoordeling, door gebruik te maken van een rolling review. Hierbij delen vaccinproducenten tijdens het klinische onderzoek al gegevens met de medicijnautoriteiten. Gedurende het proces worden nieuwe onderzoeksresultaten gedeeld met de EMA en de nationale medicijnautoriteiten (zoals het CBG). Op deze manier kunnen de medicijnautoriteiten eerder starten met de beoordeling. Dit levert tijdwinst op, zonder dat delen van het onderzoek of van de beoordeling worden overgeslagen. Voor de publiekscampagne bereiden we een animatie voor over het proces van ontwikkeling naar goedkeuring. In de paragraaf over communicatie ga ik hier verder op in.
De vaccins van AstraZeneca en BioNTech/Pfizer lijken op dit moment het meest kansrijk voor snelle beschikbaarheid, gevolgd door die van Moderna. Ondanks het feit dat voor nog geen enkel vaccin markttoelating is afgegeven, is er goede hoop dat de eerste vaccins van deze producenten in de eerste maanden van 2021 beschikbaar komen. De Europese Commissie verwacht dat tussen markttoelating en levering enkele weken kunnen zitten die producenten nodig hebben om volledig operationeel te worden. Nederland doet er alles aan om die periode zo kort mogelijk te houden. In onderstaand overzicht is weergegeven wanneer verschillende producenten verwachten hun aanvraag voor toelating te kunnen indienen.
|
Producent |
Stand van zaken klinische tests |
Verwachte aanvraag EMA-toelating |
Verwachte start levering |
|---|---|---|---|
|
AstraZeneca |
Fase III |
In de loop van 4e kwartaal 2020 |
Q1 2021 |
|
BioNTech/Pfizer |
Fase III |
In de loop van 4e kwartaal 2020 |
Q1 2021 |
|
Moderna |
Fase III |
In de loop van 1e kwartaal 2021 |
Q1/2 2021 |
|
Janssen Pharmaceuticals |
Fase III |
In de loop van 1e kwartaal 2021 |
Q2 2021 |
|
Curevac |
Fase II |
In de loop van 2e kwartaal 2021 |
Q2/3 2021 |
|
Sanofi/GSK |
Fase I/II |
In de loop van 2e kwartaal 2021 |
Q3 2021 |
Beschikbaarheid
Het is nog niet bekend welke vaccins worden toegelaten tot de markt. In de eerste maanden van 2021 is zeer waarschijnlijk sprake van beperkte beschikbaarheid, ook omdat de leveringen plaatsvinden in verschillende tranches. Dit betekent dat er dus nog niet voor iedereen vaccins zullen zijn. De afspraken met een producent bestaan steeds uit het over een periode van twee of meer kwartalen leveren van verschillende delen van het totaal overeengekomen aantal vaccins (zie tabel 2). Uiteindelijk komt het daarbij aan op de exacte leveringsschema’s waarvan op basis van daadwerkelijke productie vaccins beschikbaar komen. Als er twee partijen zijn die in het eerste kwartaal 2021 vaccins kunnen leveren, betekent dit volgens de laatste berichten van de producenten dat er ongeveer 3,5 miljoen mensen gevaccineerd kunnen worden met de eerste leveringen (die mogelijk niet allemaal tegelijk beschikbaar zijn). Voor de meeste vaccins uit het portfolio geldt dat er twee vaccins nodig zijn per te vaccineren persoon, die vermoedelijk binnen een periode van enkele weken gegeven moeten worden.
|
Bedrijf |
EU basis-levering |
3,89% aan NL = |
Hoeveel NL’ers |
Fase |
|---|---|---|---|---|
|
AstraZeneca |
300 mln |
11,7 mln |
5,8 mln |
Contract rond |
|
BioNtech Pfizer |
200 mln |
7,8 mln |
3,9 mln |
Contract rond |
|
Moderna |
80 mln |
3,1 mln |
1,6 mln |
Verk gespr rond |
|
Janssen |
200 mln |
7,8 mln |
7,8 mln |
Contract rond |
|
Curevac |
225 mln |
8,8 mln |
4,4 mln |
Contract rond |
|
Sanofi |
300 mln |
11,7 mln |
5,8 mln |
Contract rond |
Het is uiteindelijk de bedoeling dat voor iedereen in Nederland een COVID-19 vaccinatie beschikbaar is. In dit kader heb ik de Gezondheidsraad voor de zomer gevraagd te adviseren over de verschillende mogelijkheden van vaccinatie en de prioritering van verschillende doelgroepen. Dit advies, «strategieën voor COVID-19 vaccinatie», is op 19 november gepubliceerd en vormt voor het kabinet de basis om tot een vaccinatiestrategie te komen. De vaste commissie Vaccinaties van de Gezondheidsraad heeft in het advies onderzocht welke strategieën er zijn om bij beperkte beschikbaarheid van COVID-19 vaccins te kunnen prioriteren. Hierbij zijn verschillende afwegingen betrokken, omdat naast medisch-wetenschappelijke aspecten, ook ethische en maatschappelijke afwegingen een belangrijke rol spelen.
Op grond van ethische overwegingen heeft de Gezondheidsraad mogelijke doelstellingen van prioritering benoemd. Daaruit volgen vier mogelijke vaccinatiestrategieën die bij beperkte beschikbaarheid van COVID-19 vaccins kunnen worden ingezet (zie tabel 3).
|
Strategie |
Toelichting |
Doelgroepen |
|---|---|---|
|
Verminderen van (ernstige) ziekte en sterfte als gevolg van COVID-19 |
Deze strategie is gericht op het redden van zoveel mogelijk levens. Het gaat hierbij om prioriteit geven aan de groepen die een verhoogd risico lopen op ernstige ziekte of sterfte na besmetting. Daarnaast gaat het om mensen die een hoog risico lopen om deze kwetsbare groep te besmetten of zelf een hoog risico lopen op besmetting vanwege hun beroep of leefomgeving. |
• Gezondheidskundig kwetsbare groepen: 60-plussers en medische risicogroepen (in grote lijnen vergelijkbaar met groepen pandemische griep1 2009). • Groepen met verhoogd risico om mensen uit medische risicogroepen te besmetten (bijvoorbeeld zorgmedewerkers in langdurige zorginstellingen of mantelzorgers van mensen die tot een medische risicogroep behoren). • Groepen met hoger risico op infectie door beroep of leefomgeving Een eerste groep hierbij zijn de zorgmedewerkers (inclusief thuiszorg-medewerkers, ouderenzorg, langdurige zorg). Deze groep zou volgens de Gezondheidsraad verder opgedeeld kunnen worden naar medewerkers die meer of minder infectierisico lopen. • Tot slot gaat het om andere beroepen waarbij direct contact met patiënten of cliënten is en werknemers in de landbouw- en voedselindustrie. Werk-, woon- en leefomstandigheden spelen namelijk ook een rol, omdat er bijvoorbeeld geen mogelijkheden zijn tot fysiek afstand houden. |
|
Terugdringen verspreiding coronavirus |
Doel van deze strategie is het bereiken van een reproductiegetal dat lager is dan 1. Het gaat hierbij meer om indirecte bescherming van kwetsbare groepen, door je bij het vaccineren te richten op de groepen die de grootste bijdrage leveren aan verspreiding van het coronavirus (risicovormers). Dit is afhankelijk van de epidemiologische situatie en de mate waarin het beschikbare vaccin verspreiding van het virus kan tegengaan. |
Hierbij gaat het om de grootste verspreiders. Op basis van de epidemiologische situatie in het najaar van 2020 zijn dat jongeren in de leeftijdsgroep 20–30 jaar. |
|
Voorkomen maatschappelijke ontwrichting |
Bij deze strategie heeft de Gezondheidsraad niet alleen naar gezondheidsoverwegingen gekeken, maar ook naar maatschappelijke argumenten. De aandacht van de Gezondheidsraad gaat in deze strategie uit naar mensen die een belangrijke rol spelen in het draaiende houden van de samenleving. |
Groepen die van belang zijn voor het in stand houden van de zorg en behoud van vitale infrastructuur: zorgmedewerkers, onderwijs, openbare orde, openbaar bestuur. Hierbij gaat allereerst aandacht uit naar de zorgsector, vanuit een andere doelstelling dan bij strategie 1. |
|
Combinatiestrategie |
Twee of drie van bovenstaande doelstellingen worden gecombineerd, bijvoorbeeld het voorkomen van ernstige ziekte en sterfte en het overeind houden van vitale sectoren, zoals de zorg. |
Vergt nadere prioritering op basis van de verschillende doelstellingen. |
Het gaat hierbij om patiënten met afwijken en functiestoornissen van de luchtwegen en longen, patiënten met chronische hartklachten, diabetes mellitus, patiënten met chronische nierinsufficiëntie, patiënten met een afweerstoornis of behandeld met immuunsuppressiva die leiden tot verminderde weerstand tegen luchtweginfecties, mensen met een verstandelijke beperking wonend in instellingen, en verpleeghuisbewoners.
De Gezondheidsraad adviseert op basis van de huidige (epidemiologische) situatie, waarin de druk op de zorg onverminderd hoog is en kwetsbare mensen nog steeds zwaar worden getroffen door (de gevolgen van) COVID-19, te starten met het vaccineren van ouderen boven de 60 jaar en medische risicogroepen (strategie 1). Als er binnen deze groepen mensen zijn die om medische redenen niet zelf gevaccineerd kunnen worden, adviseert de Gezondheidsraad de zorgmedewerkers en mantelzorgers die een besmettingsrisico voor hen vormen te vaccineren. Bij beperkte beschikbaarheid van vaccins komt de Gezondheidsraad, binnen deze strategie, tot de volgende prioritering:
• Ouderen vanaf 60 jaar die tot medische risicogroepen behoren, te beginnen met de oudste leeftijdsgroep, omdat daar het risico op ernstige ziekte en sterfte het grootst is. Met een medische indicatie worden ook mensen met een verstandelijke beperking die in een instelling wonen, en verpleeghuisbewoners bedoeld;
• Overige mensen van 60 jaar en ouder, te beginnen met de oudste leeftijdsgroepen. Omdat herinfecties mogelijk zijn, komen ook ouderen die al een infectie hebben doorgemaakt in aanmerking.
• Mensen onder de 60 jaar die tot medische risicogroepen behoren;
• De Gezondheidsraad geeft aan dat er ook kwetsbare mensen zijn die om medische redenen niet gevaccineerd kunnen worden. In dat geval is het ook belangrijk om de mantelzorgers en zorgmedewerkers die een risico voor ze vormen te vaccineren. In aanvulling op bovenstaande groepen noemt de Gezondheidsraad hier ook zorgmedewerkers met direct patiëntcontact.
De Gezondheidsraad schat in dat voor het vaccineren van alle ouderen (60-plussers) en medische risicogroepen in ieder geval 5 miljoen vaccins nodig zijn (en 10 miljoen bij twee vaccinaties). Aanvullend hierop gaat het om circa 1,5 miljoen zorgmedewerkers in verpleeghuizen, de thuiszorg, langdurige zorg, en mantelzorgers die contact hebben met medische risicogroepen.
De Gezondheidsraad benadrukt dat het hier om een voorlopig advies gaat. Volgens de commissie hangt de te kiezen strategie sterk af van de epidemiologische situatie en de werking van vaccins. Dat maakt het volgens de Gezondheidsraad lastig om uitspraken te doen over de situatie over drie of zes maanden. Zodra nieuwe informatie beschikbaar komt zal de Gezondheidsraad een nader advies uitbrengen over de inzet van vaccins.
Ik heb grote waardering voor het zorgvuldige advies dat door de Gezondheidsraad is opgesteld. Door ouderen en mensen uit medische risicogroepen als eerst te vaccineren, kunnen we ernstige ziekte en sterfte als gevolg van het coronavirus zoveel mogelijk voorkomen. Dat sluit aan bij de doelstellingen die het kabinet heeft geformuleerd om het virus te bestrijden: het beschermen van kwetsbaren en voorkomen dat de zorg verder overbelast raakt. Het kabinet neemt het advies van de Gezondheidsraad daarom over. Niet alleen omdat deze strategie vanuit epidemiologisch perspectief het meest voor de hand ligt, ook sociaal-maatschappelijke en economische overwegingen spelen hierbij een rol. Hoe eerder we in staat zijn om kwetsbare mensen te beschermen tegen het virus, hoe sneller we de meest beperkende maatregelen achter ons kunnen laten.
De aanbevelingen die de Gezondheidsraad doet, sluiten aan ook goed bij de adviezen van de Strategic Advisory Group of Experts on Immunization (SAGE) van de WHO en het ECDC, en de recent gepresenteerde Vaccinatiestrategie van de Europese Unie. Ook ons omringende landen als Denemarken, Duitsland en het Verenigd Koninkrijk maken vergelijkbare keuzes. Die aansluiting is belangrijk, omdat bestrijding van de pandemie een gezamenlijke opgave is.
Hoofdroute
Het kabinet wil starten met het vaccineren van ouderen (60-plussers), medische risicogroepen, en zorgmedewerkers die met deze groepen in contact komen. Dit is een grote groep mensen voor wie snelle beschikbaarheid van een COVID-19 vaccin belangrijk is. Omdat er in de eerste maanden zeer waarschijnlijk sprake is van beperkte hoeveelheden vaccins, zullen we ook binnen deze groepen een verdere prioritering moeten aanbrengen. Dat doen we door te beginnen met die groepen waar de kans op ernstige ziekte en overlijden het hoogst is.
Het kabinet kiest ervoor de eerste vaccins beschikbaar te stellen aan bewoners van verpleeghuizen. Het gaat om circa 130.000 mensen die intramuraal verblijven, en tussen de 20.000 en 25.000 mensen in verscheidene woonvormen, die soms niet van een verpleeghuis te onderscheiden zijn. Daarnaast gaat het ook om alle mensen met een verstandelijke beperking wonend in een instelling, zoals geadviseerd door de Gezondheidsraad. Bij mensen die vanwege onderliggend lijden niet gevaccineerd kunnen worden, adviseert de Gezondheidsraad om in te zetten op «ringbescherming»: het beschermen van mensen in de nabijheid van een kwetsbaar persoon, om zo toch de kans op besmetting en ziekte te verkleinen. Omdat dit onderscheid lastig te maken is in verpleeghuizen en instellingen voor mensen met een verstandelijke beperking, vaccineren we ook alle medewerkers. In het geval van de verpleeghuizen gaat het in ieder geval om 265.000 medewerkers. Ik zal daarnaast met de instellingen nader overleg voeren over de wijze waarop mantelzorgers bij de vaccinaties kunnen worden meegenomen.
Na deze eerste groep volgen andere groepen zoals: 60-plussers met een medische indicatie (beginnend met de oudste leeftijdsgroepen), 60-plussers zonder medische indicatie (waarbij ook hier de oudste leeftijdscategorieën het eerst in aanmerking komen), mensen onder de 60 jaar met een medische indicatie, de zorgmedewerkers van deze groepen, én de zorgmedewerkers die in direct contact staan met patiënten met COVID-19.
Naarmate meer vaccins worden geleverd, kunnen groepen worden toegevoegd: andere medewerkers in de zorg en tot slot ook de groep mensen onder de 60 jaar zonder een medische indicatie. Binnen deze groep kan ook nader worden geprioriteerd. Daarbij kijken we enerzijds naar het verminderen van verspreiding van het virus (de epidemiologische situatie), en anderzijds naar het in stand houden van vitale sectoren. Uiteindelijk is het de bedoeling dat iedereen in Nederland gevaccineerd kan worden tegen het coronavirus.
Pas op het moment dat de vaccins worden goedgekeurd, weten we zeker dat de vaccins geschikt zijn voor een bepaalde doelgroep. Onze aanpak en strategie moeten daarom wendbaar zijn. In dit kader werk ik samen met uitvoerende partijen meerdere scenario’s uit, waarbij ook aandacht is voor een nadere definiëring en invulling van de hierboven genoemde groepen. Ik houd u op de hoogte van de vorderingen via de voortgangsbrief. We verwachten met deze hoofdstrategie te kunnen starten in januari, maar we houden ook rekening met eerste beschikbaarheid in december.
Figuur 1. Stappen in hoofdroute vaccinatiestrategie
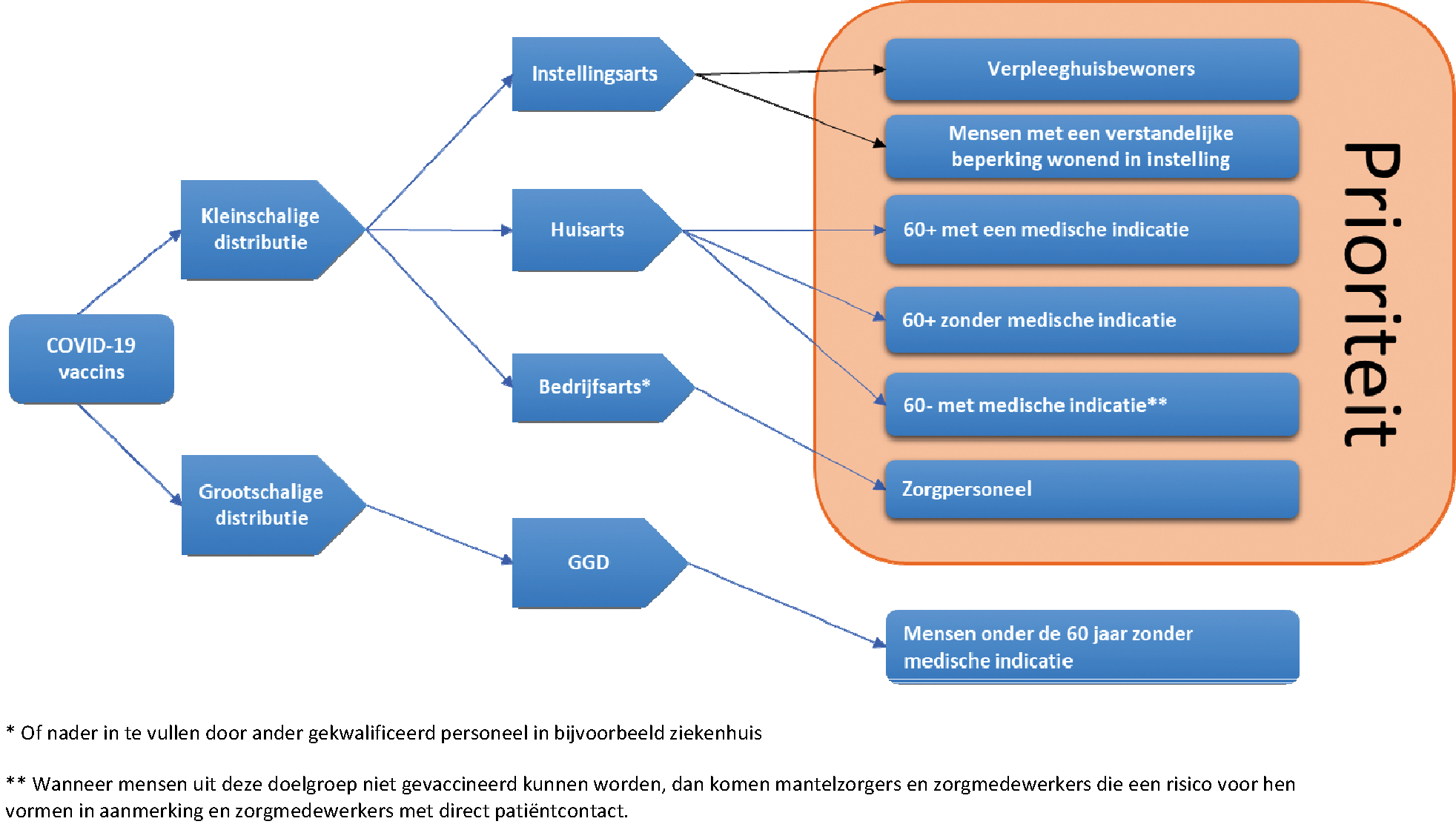
Aandachtspunten
De COVID-19-vaccinatie is een complex traject met veel afhankelijkheden, die op dit moment nog niet allemaal bekend zijn. Dat heeft impact op hoe de strategie er in de dagelijkse praktijk uitziet. De uiteindelijke keuzes die we maken hangen samen met de geschiktheid van een vaccin voor een specifieke groep, en informatie over de mate waarin een vaccin verspreiding kan verminderen. Dit zal blijken uit de definitieve testresultaten en bij de beoordeling voor toelating van een kandidaat-vaccin.
De volgende variabelen kunnen ertoe leiden dat het kabinet moet kiezen voor een aanpassing van de hoofdroute:
i. De geschiktheid van vaccins voor specifieke doelgroepen
Niet alle vaccins zullen geschikt zijn voor elke groep. Pas als vaccins door de EMA en het CBG zijn goedgekeurd, weten we voor welke groepen een vaccin ingezet kan worden. Over de geschiktheid van kandidaat-vaccins voor specifieke groepen adviseert de Strategic Advisory Group of Experts on Immunization (SAGE) van de WHO zodra de vaccins beschikbaar komen (verwachting is binnen twee weken na markttoelating). Mogelijk zal ook de Gezondheidsraad om een aanvullend advies gevraagd worden.
ii. De aantallen die steeds beschikbaar komen
In welke mate een of meerdere prioritaire groepen tegelijkertijd gevaccineerd kunnen worden, hangt af van de beschikbare hoeveelheid vaccins. Het ontvangen van kleinere tranches betekent namelijk dat we tot een nog specifiekere indeling moeten komen. Uiteraard ontstaat meer ruimte naarmate het aantal kandidaat-vaccins wat beschikbaar komt hoger is en ook de productie tijdig en goed functioneert.
iii. De wijze waarop de vaccins worden geleverd
De eigenschappen van de verschillende typen kandidaat-vaccins zijn van invloed op de logistieke voorbereidingen. Zo moet het van BioNTech/Pfizer bijvoorbeeld op -70°C bewaard worden, en dat stelt eisen aan de organisatie van de toediening. Ook het aantal vaccins wat per eenheid verpakt zit maakt dat sommige vaccins meer of minder geschikt zijn voor bijvoorbeeld kleinschalige toediening.
Samenvattend gaat het om het gebruik van het juiste vaccin, voor de juiste toepassing, in de juiste fase. Op het moment dat meer gegevens – zoals definitieve resultaten uit de laatste fase van het klinisch onderzoek – beschikbaar zijn, moet de hoofdroute aangepast kunnen worden op basis van de laatste inzichten. Dit doen we samen met het RIVM en andere betrokken partijen. Het RIVM zal de situatie hiertoe wekelijks in kaart brengen.
Vaccinatie langere termijn
Ook op de langere termijn willen we samenleving kunnen beschermen tegen het virus. Het is afhankelijk van onder meer de duur van de immuniteit, de circulatie van het virus en deelname aan het vaccinatieprogramma hoe dit het beste bewerkstelligd kan worden. Op dit moment is nog weinig bekend over de beschermingsduur van vaccins. We houden daarom rekening met de mogelijkheid dat de COVID-19 vaccinatie een jaarlijks terugkerende vaccinatiecampagne moet worden, net als bij de griepprik.
Startdatum en samenhang maatregelen
Afhankelijk van wanneer een geregistreerd vaccin beschikbaar komt, zal een startdatum bepaald worden. De verwachting is op z’n vroegst begin 2021, vanwege het de nog lopende onderzoeken, de beoordelingsprocedure, en het gereed maken van de leveringen. We bereiden ons ook voor op een scenario waarin al in december vaccins worden geleverd.
De stap naar vaccinatie is ook een stap om het virus beter onder controle te krijgen en het weer openen van de samenleving. Evenals de uitbreiding van het aantal testen. Het is van belang om te kijken wat vaccinatie betekent voor de beperkende maatregelen die we op dit moment hebben genomen. In dat kader zal het kabinet het OMT vragen mede aan de hand van de epidemiologische situatie zijn visie te geven op de verhouding tussen de vaccinatie en de huidige maatregelen.
Het RIVM werkt aan een landelijk registratiesysteem speciaal voor de COVID-19-vaccinatie. Het centrale register is een noodzakelijk onderdeel van de vaccinatiestrategie, en belangrijk in het kader van de veiligheidsbewaking en monitoring van bijwerkingen, het snel handelen bij eventuele calamiteiten, en de bestrijding van de pandemie. Het is heel belangrijk dat de gegevens in het centrale register zo compleet mogelijk zijn zodat de veiligheidsbewaking en monitoring zorgvuldig kan gebeuren. Hierbij heb ik privacy hoog in het vaandel staan en acht ik het van belang dat het register voldoet aan de privacy wet- en regelgeving. Daarbij is van betekenis dat de registratie zal bestaan uit niet meer dan de minimale benodigde gegevens zoals wie, wanneer, welk vaccin heeft gekregen en worden de privacy by design principes als uitgangspunt genomen. Desondanks kan het zo zijn dat iemand bezwaar heeft op het verwerken van zijn/haar gegevens door het RIVM, in dat geval zal het mogelijk zijn voor de gevaccineerde om zijn/haar gegevens bij het RIVM te laten verwijderen. Het zal gaan om minimale gegevens zoals wie, wanneer, welk vaccin heeft gekregen. Ik wil graag benadrukken dat het niet alleen voor ieders eigen veiligheid, maar ook voor de veiligheid van anderen wenselijk is om deze minimale set aan gegevens bij het RIVM te laten registreren. De registratie is essentieel voor het individuele belang van gevaccineerde, maar ook van publiek maatschappelijk belang dat het RIVM zijn rol ten aanzien van de vaccinatie in de bestrijding van de pandemie optimaal kan uitvoeren.
Er wordt hard gewerkt aan de technische uitvoering van het centrale register. Hierbij zal worden aangesloten op de systematiek en infrastructuur van het Rijksvaccinatieprogramma en wordt ingezet op het zoveel mogelijk beperken van de administratieve lasten voor de uitvoerders.
We maken gebruik van de systematiek en infrastructuur van een bestaand systeem, zodat er zo snel mogelijk een centraal register gereed is. Dit systeem kan gebruikt worden voor het monitoren van de vaccinatiegraad, de veiligheid en de effectiviteit.
Het Ministerie van VWS heeft de opdracht aan het RIVM gegeven voor voorbereiding en uitvoering van de COVID-19-vaccinatie. Hierbinnen valt ook de regie op de uitvoering van de vaccinatie door uitvoerende partijen, zoals huisartsen en de GGD. Vooruitlopend op het advies van de Gezondheidsraad, heeft het RIVM – in opdracht van VWS – een scenarioverkenning uitgevoerd naar de mogelijke partijen die een rol kunnen spelen bij de uitvoering van de COVID-19 vaccinatie. Normaal gesproken brengt het RIVM pas na advisering door de Gezondheidsraad de uitvoeringsaspecten, zoals mogelijke uitvoerende partijen en de daarbij komende kosten, in kaart.
Vanwege de hoge urgentie heeft het RIVM nu al een verkenning gedaan waarin beschreven is hoe de uitvoering op een efficiënte en laagdrempelige manier uitgevoerd kan worden. Er zijn verschillende uitvoerende partijen in beeld:
• Huisartsen voor de medische risicogroepen en ouderen (extramuraal);
• Instellingsartsen voor medische risicogroepen en ouderen (intramuraal);
• Werkgevers en arbodiensten/bedrijfsartsen voor zorgpersoneel; en,
• GGD’en voor de rest van de bevolking en eventueel als vangnet voor bovenstaande doelgroepen.
Het RIVM heeft geadviseerd om de vaccinatie door bovengenoemde partijen te laten uitvoeren, omdat daarmee zoveel mogelijk wordt aangesloten op de reeds bestaande structuren van bijvoorbeeld de griepvaccinatie en daarmee snel en op een zo efficiënt mogelijke wijze kan worden gewerkt. Om geen kostbare tijd te verliezen en om – ook in deze fase waarin nog veel onbekend is – zo goed mogelijk voorbereid te zijn, werkt het RIVM sinds de zomer ook hard aan de praktische implementatie.
Het Ministerie van VWS heeft in de afgelopen periode initiatief genomen en partijen bijeengebracht voor deze opgave. In de komende periode zal VWS, ondersteund door onder meer het RIVM, met hen verdere afspraken maken over de inrichting van de samenwerking. Op deze manier kan elk van de partijen vanuit de eigen kennis en kunde haar bijdrage leveren aan een succesvolle vaccinatiecampagne. Zo ben ik met de LHV (huisartsen) in gesprek over de het selecteren, uitnodigen en vaccineren van 60-plussers en medische risicogroepen (extramuraal)6 en met Actiz, Verenso, VGN, Zorgthuisnl, V&VN en de NVAVG over de vaccinatie van medische risicogroepen die zich intramuraal bevinden. Ik ben ook met de werkgevers van zorgpersoneel en de OVAL en NVAB (arbodiensten/bedrijfsartsen) in gesprek over de selectie, uitnodiging en vaccinatie van zorgpersoneel en met de GGD’en over de vaccinatie van andere groepen. Groepen die door de GGD’en worden gevaccineerd zullen vanuit het RIVM geselecteerd worden en een uitnodiging hiervoor ontvangen.
De onbekendheden rondom de beschikbaarheid en geschiktheid van vaccins voor specifieke doelgroepen hebben ook invloed op de voorbereidingen die uitvoerende partijen treffen. Daarom werken we samen met de uitvoerende partijen verschillende scenario’s uit. Hierbij is onder andere aandacht voor het inrichten van ondersteunende IT-systemen en afspraken over de distributie van vaccins en het inrichten van vaccinatielocaties. Ook werken betrokken partijen aan het opstellen van richtlijnen en een e-learning, ten behoeve van de deskundigheidsbevordering van de professionals.
Bij de uitvoering wil ik zoveel als mogelijk gebruik maken van de bestaande structuren, en voor de betreffende doelgroepen vertrouwde, locaties. Hierbij wordt zoveel mogelijk aangesloten bij de structuur van de griepvaccinatie en dat is daarmee een bekende route voor de betreffende doelgroep. Werkgevers kunnen die vaccinatie zelf aanbieden, of in samenwerking met de arbodiensten. GGD’en kunnen gebruik maken van grootschalige priklocaties zoals zij doen bij de HPV-vaccinatie en de meningokokkenvaccinatie of kleinere locaties waar nodig. Mogelijk dat de GGD te zijner tijd hun (grote) testlocaties ook hiervoor kunnen inzetten.
We bereiden ons voor op het scenario dat in januari landelijk gestart wordt met vaccineren. In de voorbereidingen is ook rekening gehouden met de mogelijkheid dat in december al de eerste vaccins beschikbaar zijn.
Het mag duidelijk zijn dat (ook) de uitvoering een grote en complexe uitdaging is. Voor alle betrokken partijen. Daarom hebben we ieders inzet en deskundigheid hard nodig. Het is fijn te weten dat er veel positieve energie is om deze uitdagende klus met elkaar vorm te geven. Dat blijkt ook uit de hulp die wordt aangeboden, zoals die van het Rode Kruis. Ik ben daar blij mee en ben met ze in gesprek over de bijdrage die zij willen en kunnen leveren.
Uitvoering Caribisch Nederland
Nederland heeft afgesproken dat ook de Caribische delen van het koninkrijk meedelen in de aantallen die voor Nederland beschikbaar komen. Op dit moment wordt samen met vertegenwoordigers van de BES- en de CAS-eilanden geïnventariseerd wat nodig is om ook op het Caribisch deel van Nederland een goede vaccinatiecampagne op te kunnen zetten. De Gezondheidsraad zal op verzoek van CAS-eilanden een advies uitbrengen over de prioritering van doelgroepen in deze delen van het koninkrijk. Dit advies wordt naar verwachting in december opgeleverd. Voor de verdere voorbereidingen is met name de logistieke organisatie een cruciaal onderdeel. Afgesproken is dat de BES- en CAS-eilanden zelf verantwoordelijk zijn voor de opslag en distributie van vaccins op de eilanden zelf. Zij bereiden zich in dit kader voor op verschillende scenario’s. Het RIVM heeft hierbij een adviserende rol en controleert of aan de randvoorwaarden voor correct vaccinbeheer wordt voldaan.
We treffen volop voorbereidingen voor het logistieke proces. Hierbij maken we gebruik van de ervaring die we hebben opgedaan met de vaccinatie tegen pandemische griep. Het betreft hier echter een unieke logistieke operatie, mede vanwege de grote diversiteit in aangekochte vaccins.
Naast de eigenschappen van de verschillende typen vaccins die invloed hebben op de opslag, verpakking, en het transport, spelen ook de leveringstermijnen een rol. De meest kansrijke kandidaat-vaccins en de verwachte leveringstermijnen die daarbij worden verwacht, zijn nu leidend in het tijdpad van onze voorbereidingen.
Zo werkt het RIVM aan het tijdig beschikbaar hebben van voldoende koel- en vriescapaciteit. Met name dat laatste is een ingewikkelde operatie omdat er ook vaccins worden ontwikkeld die een erg lage opslagtemperatuur vereisen. De faciliteiten voor diepgevroren vaccins (–70 graden) zijn eind december gereed. Ook heeft het RIVM momenteel 25 miljoen extra veiligheidsnaalden en spuiten ingekocht voor de toediening van de COVID-19 vaccins. In aanvulling daarop doet Nederland mee in de Joint Procurement van de Europese Commissie voor de aanschaf van veiligheidsnaalden.
Gezien het nationale belang van de vaccins wordt ook gekeken naar veiligheidsaspecten van het gehele logistieke proces. Een overheidsbrede werkgroep, geleid door het Ministerie van VWS en het RIVM, werkt alle onderliggende afspraken nader uit zodat de vaccins veilig binnen Nederland kunnen worden vervoerd, opgeslagen, en kunnen worden toegediend. Daarbij is vanzelfsprekend ook contact met lokale partijen, leveranciers, logistieke partijen etc. Het gaat hierbij niet alleen om security, maar ook om safety.
Belangrijke pijlers in deze vaccinatiestrategie zijn de publiekscommunicatie en de dialoog met de samenleving. Zo informeren we het algemeen publiek over het vaccin en de vaccinatie-aanpak. Hierin hebben we uiteraard ook aandacht voor speciale doelgroepen die specifieke behoefte hebben in vorm, taal, kanaal of afzenderschap (bijvoorbeeld overheid, via koepels of via de eigen zorgverlener, enz.) Dit betreft bijvoorbeeld jongeren, mensen met een laag sociaaleconomische status, laaggeletterden en anderstaligen.
Omdat de COVID-19 vaccins ook vragen, twijfels en emoties oproept, zetten we extra in op het beantwoorden van die vragen en het ingaan op twijfels, het weerspreken van desinformatie en het steeds weer verwijzen naar de feitelijk juiste informatie. We gaan daartoe waar mogelijk in gesprek om te horen over twijfels en ideeën die er leven, en om te kunnen informeren of verwijzen, en geruststellen waar dat kan.
Zo snel mogelijk starten we ook met middelen om grote groepen te bereiken, waaronder televisie en radio. Nu steeds meer informatie beschikbaar komt over de COVID-19 vaccinatie, is het belangrijk om de samenleving hier goed van op de hoogte te houden. Het zal hierbij gaan om een concreet handelingsperspectief, maar ook over de samenhang tussen maatregelen en verschillende instrumenten die we inzetten om het coronavirus onder controle te krijgen. We gaan mensen tegelijkertijd motiveren voor de vaccinatie en hen activeren ook daadwerkelijk gebruik te maken van een mogelijk aanbod. Dat het belangrijk is om hier vol op in te zetten blijkt ook uit verschillende recente onderzoeken van bijvoorbeeld Ipsos en de gedragsunit van het RIVM. Zij schetsen dat de vaccinatiebereidheid varieert van 50–71%. Uit onderzoek van de TU Delft blijkt dat de meerderheid van de Nederlanders zich niet direct wil laten vaccineren en blijken er bij zorgpersoneel twijfels zijn over de vaccinatie.
Dat is zorgelijk, omdat een succesvol vaccin een belangrijk instrument is in de aanpak van het virus: naast individuele bescherming zorgen vaccins ervoor dat je ook de groep beschermt, als voldoende mensen zich laten vaccineren En daarom moeten we het goede gesprek voeren over vragen en zorgen van alle mensen zo goed mogelijk adresseren, het belang van vaccineren uitleggen en daar helder en eerlijk over communiceren.
Communicatie naar deze te vaccineren groepen neemt het RIVM op zich, net als de communicatie naar zorgprofessionals als uitvoerder van de vaccinaties.
Deze aanpak moet ertoe leiden dat mensen weten waar ze betrouwbare informatie kunnen vinden en geholpen worden, en het draagvlak voor de belangrijke keuzes die hier moeten worden gemaakt voldoende groot blijft. Uiteraard wordt de communicatie voortdurend bijgesteld op basis van de ontwikkelingen van de vaccins en de keuzes die nog moeten worden gemaakt.
Het monitoren van de vaccinatiegraad, de effectiviteit, en mogelijke bijwerkingen van de COVID-19 vaccinatie, is in deze pandemie en bij deze vaccins cruciaal. Gezien de bijzondere maatschappelijke omstandigheden en de impact die het coronavirus heeft, wordt hier extra op ingezet. Het RIVM werkt de inzet op onderzoek, monitoring en veiligheidsbewaking samen met andere partijen uit. Om deze taak uit te kunnen voeren is het verkrijgen van vaccinatiegegevens via het landelijke registratiesysteem van belang.
Het College ter Beoordeling van Geneesmiddelen (CBG) heeft, naast een rol bij de beoordeling en toelating van het vaccin, ook een verantwoordelijkheid voor de geneesmiddelenbewaking. Het CBG heeft een prominente rol binnen het Europese netwerk als deelnemer aan de COVID-19 EMA Pandemic Task Force (COVID-ETF). Deze taskforce richt zich onder andere op:
• Het evalueren van de beschikbare wetenschappelijke gegevens over COVID-19-geneesmiddelen en het identificeren van veelbelovende kandidaten;
• Het geven van wetenschappelijk advies aan geneesmiddelen- en vaccinontwikkelaars met betrekking tot de klinische studies voor registratie, risk management, en post-marketing follow up.
• Het stroomlijnen van het registratie- en beoordelingsproces, onder andere in samenwerking met vaccinontwikkelaars, public health organisaties, en academische instellingen.
Onderzoek naar mogelijke bijwerkingen
Onderdeel van de geneesmiddelenbewaking is ook het verzamelen, vastleggen en analyseren van meldingen van (vermoedelijke) bijwerkingen. Dat gebeurt door professionals uit de zorg en door patiënten zelf. Zoals ik eerder in mijn brief van 23 september jl. heb aangegeven, heeft Bijwerkingencentrum Lareb hierbij een belangrijke rol (in opdracht van het CBG). In dit kader werkt Bijwerkingencentrum Lareb aan de technische voorbereidingen om vanaf januari klaar te zijn voor het ontvangen en verwerken van meldingen van eventuele bijwerkingen. Zo is er een specifiek COVID-19 meldformulier ontwikkeld. Daarnaast worden analysetools, en formats voor rapportages en overlegstructuren ontwikkeld om snel en effectief veiligheidsproblemen op te sporen, zowel voor nieuwe (ernstige) bijwerkingen, als het in kaart brengen van het patroon en frequenties van de te verwachte bijwerkingen. Ook is gestart met de werving van extra personeel. Tot slot werkt het Lareb in het kader van actieve veiligheidsbewaking aan een (web)applicatie om groepen mensen vrijwillig actief te volgen om bijwerkingen te monitoren: Lareb Intensive Monitoring (LIM). Gevaccineerde personen worden hierbij uitgenodigd om online korte vragenlijsten in te vullen over eventuele bijwerkingen na vaccinatie. Deze mensen worden zes maanden gevolgd, waarbij het per vaccin om minstens 5000 gevaccineerde deelnemers gaat. Door in te zetten op dit soort actieve monitoring, zijn we sneller op de hoogte van mogelijke bijwerkingen. Bij een nieuw vaccin is dit extra belangrijk.
Europees onderzoek
Op Europees niveau is er een voorbereidingsproject (ACCESS) gestart, dat wordt gefinancierd door de EMA. Dit project wordt geleid door de Universiteit Utrecht en zowel het RIVM als Bijwerkingencentrum Lareb nemen hieraan deel. Binnen dit project wordt onderzoek voorbereid om de effectiviteit, het aantal vaccinaties en de veiligheid van de vaccinaties te kunnen bestuderen vanaf het moment dat vaccins gebruikt gaan worden. Daarnaast worden in dit EU-project afspraken gemaakt over gezamenlijke onderzoeks-infrastructuur om de bewaking van de veiligheid van deze vaccins in Europa uit te voeren. Doel is om in december 2020 een Europese infrastructuur gereed te hebben.
Goed zicht en vroegtijdige informatie zijn belangrijk, zeker in een context waarin mogelijk verschillende vaccins in omloop zijn. Ook is een goede registratie essentieel omdat mensen bij de meeste kandidaten twee vaccinaties ontvangen. Bijwerkingencentrum Lareb, het RIVM, en het CBG werken daarom nauw samen rondom de veiligheidsbewaking. Mocht er ondanks alle voorzorg onverhoopt sprake zijn van enige calamiteit met een vaccin, dan kan daarop snel geïntervenieerd worden, door bijvoorbeeld te herleiden om welke batch het gaat.
Aankoop
Gedurende het aankooptraject zijn strenge afspraken gemaakt over geheimhouding. Er is een geheimhoudingsplicht ingesteld om te voorkomen dat onze onderhandelingspositie ten overstaande van de verschillende producenten op negatieve wijze wordt beïnvloed en omdat de contracten bedrijfsvertrouwelijke en beursgevoelige informatie van de producent bevatten die niet openbaar mag worden. Tegelijk wil ik uw Kamer ook zoveel mogelijk informeren over de afspraken en keuzes die worden gemaakt, voor zover dit binnen de vertrouwelijkheidsvereisten mogelijk is.
Het kabinet heeft eerder een budget van € 700 miljoen ter beschikking gesteld voor de aankoop van vaccins tegen het coronavirus. Zoals ik eerder in deze brief heb aangegeven worden deze vaccins in gezamenlijkheid met de overige EU-lidstaten ingekocht, op basis van door de Europese Commissie te sluiten Advanced Purchase Agreements (APA). Om deze overeenkomsten mogelijk te maken doet de Europese Commissie een voorfinanciering vanuit het Emergency Support Instrument (ESI). Deze overeenkomsten leiden tot een afnamerecht tegen een vaste (lagere) prijs voor de lidstaten, op basis van hun aandeel in het inwoneraantal van de Europese Unie (pro rata). Het Nederlandse deel beslaat 3,89%. Nederland is verplicht die vaccins af te nemen, zodra de producent hiervoor een markttoelating heeft verkregen.
Onderstaand een indicatieve begroting rond de vaccininkoop. Aangezien nog niet alle overeenkomsten gesloten zijn, betreft het hier een eerste inschatting. We gaan daarbij uit van de aanschaf van in ieder geval zes, en mogelijk zeven verschillende vaccins.
|
Begroting aankoop vaccins |
|
|---|---|
|
Kosten aankoop vaccins portfolio van 6 (en reservering 7) |
€ 490 miljoen |
|
Kosten aanvullende financiering ESI-Budget |
€ 43 miljoen |
|
Bijdrage COVAX ten behoeve van kwetsbare landen |
€ 25 miljoen |
|
Kosten aankoop vaccins aanvullende portfolio |
€ 109 miljoen |
|
Totaal |
€ 667 miljoen |
1) Betreft de kosten van de aankoop van vaccins uit de Europese portfolio bestaande uit AstraZeneca, BionTech/Pfizer, Sanofi/GSK, Johnson&Johnson, Moderna, Curevac en mogelijk een zevende kandidaat.
2) Betreft de Nederlandse bijdrage aan de noodzakelijke verhoging van het ESI budget voor het doen van de voorinvesteringen.
3) Betreft de Nederlandse bijdrage aan Covax, het mondiale initiatief voor de beschikbaarheid van vaccins voor kwetsbare landen.
4) Betreft de mogelijke aankoop van vaccins van een viertal andere vaccinproducenten.
Ik besef dat het hier gaat om forse investeringen. De risico’s die gepaard gaan met het investeren in dergelijke ontwikkeltrajecten wegen echter niet op tegen het zeer grote maatschappelijke belang om snel te kunnen beschikken over veilige en effectieve vaccins.
Uitvoeringskosten
Naar verwachting bestaat de grootste kostenpost van het implementatietraject uit de vergoeding die de uitvoerders zullen ontvangen voor de verrichtingen. Daarnaast worden gemaakt voor bijvoorbeeld distributie, opslag, toedieningsmaterialen, veiligheidsbewaking en het centrale registratie inclusief het beheer daarvan. De eerste ramingen voor de implementatie van de COVID-19 vaccins worden op dit moment geschat op 900 miljoen tot 1 miljard euro. In de ramingen wordt uitgegaan van twee doses vaccin.
Tot slot
Het ontwikkelen van een nationale vaccinatiestrategie brengt veel uitdagingen met zich mee, met name omdat er nog veel onbekend is over de nieuwe vaccins. De belangrijkste stappen hebben we in beeld: vaccins moeten een grondige toelatingsprocedure doorlopen voordat ze mogen worden gebruikt, er moet een zorgvuldig onderbouwde prioritering van doelgroepen zijn, en de uitvoering van de vaccinatie moet hierop worden aangesloten. Waar mogelijk maken we daarbij gebruik van bestaande structuren. Tegelijkertijd kent deze operatie unieke kenmerken, die vragen om een groot aanpassingsvermogen van alle betrokken partijen. Er wordt door deze partijen ontzettend hard gewerkt om zo snel mogelijk na de eerste leveringen van COVID-19 vaccins te kunnen starten met het daadwerkelijk vaccineren van de samenleving. Hierbij werken we nauw samen met andere Europese landen, zowel voor de aankoop van de vaccins als bij het voorbereiden van de vaccinatiecampagne. Hoewel de gezondheidssystemen per land verschillen, zien we dat bij alle lidstaten dezelfde vragen spelen over logistiek, uitvoering, registratie, monitoring en veiligheidsbewaking.
Vanzelfsprekend wisselen we deze ervaringen ook uit op Europees niveau, en kijken we op welke manieren we elkaar daarbij kunnen ondersteunen. Naast het verder uitwerken van bovengenoemde stappen dient, gezien de maatschappelijke impact, veel aandacht te zijn voor transparante, toegankelijke en duidelijke informatie waarbij oog is voor vragen en zorgen vanuit de samenleving. Ook ethische afwegingen spelen hierbij een rol.
De Minister van Volksgezondheid, Welzijn en Sport, H.M. de Jonge
Onder andere WHO SAGE Roadmap for prioritizing uses of COVID-19 vaccines in the context of limited supply (https://www.who.int/publications/m/item/who-sage-roadmap-for-prioritizing-uses-of-covid-19-vaccines-in-the-context-of-limited-supply), Mededeling Voorbereiding van COVID-19-vaccinatiestrategieën en inzet van COVID-19-vaccins van de Europese Commissie (https://eur-lex.europa.eu/legal-content/nl/ALL/?uri=CELEX:52020DC0680), ECDC: Key aspects regarding the introduction and prioritisation of COVID-19 vaccination in the EU/EEA and the UK (https://www.ecdc.europa.eu/sites/default/files/documents/Key-aspects-regarding-introduction-and-prioritisation-of-COVID-19-vaccination.pdf).
Kopieer de link naar uw clipboard
https://zoek.officielebekendmakingen.nl/kst-25295-745.html
De hier aangeboden pdf-bestanden van het Staatsblad, Staatscourant, Tractatenblad, provinciaal blad, gemeenteblad, waterschapsblad en blad gemeenschappelijke regeling vormen de formele bekendmakingen in de zin van de Bekendmakingswet en de Rijkswet goedkeuring en bekendmaking verdragen voor zover ze na 1 juli 2009 zijn uitgegeven. Voor pdf-publicaties van vóór deze datum geldt dat alleen de in papieren vorm uitgegeven bladen formele status hebben; de hier aangeboden elektronische versies daarvan worden bij wijze van service aangeboden.
