Kamerstuk
| Datum publicatie | Organisatie | Vergaderjaar | Dossier- en ondernummer |
|---|---|---|---|
| Tweede Kamer der Staten-Generaal | 2018-2019 | 29447 nr. 44 |
Zoals vergunningen, bouwplannen en lokale regelgeving.
Adressen en contactpersonen van overheidsorganisaties.
U bent hier:

| Datum publicatie | Organisatie | Vergaderjaar | Dossier- en ondernummer |
|---|---|---|---|
| Tweede Kamer der Staten-Generaal | 2018-2019 | 29447 nr. 44 |
Aan de Voorzitter van de Tweede Kamer der Staten-Generaal
Den Haag, 4 oktober 2018
Met deze actualiteitenbrief informeer ik u over de ontwikkelingen in de bloedvoorziening van het afgelopen jaar. Tegelijkertijd stel ik voor 2019 de prijzen vast van plasma als grondstof voor plasmageneesmiddelen. Onlangs heeft de Gezondheidsraad het advies Testen van bloeddonaties op hepatitis E-virus1 aan uw Kamer aangeboden. In deze brief reageer ik tevens op dit rapport.
In de Wet inzake bloedvoorziening is vastgelegd dat ik het parlement driejaarlijks een ministerieel plan stuur over de bloedvoorziening. In de tussenliggende jaren informeer ik het parlement door middel van een actualiteitenbrief. Dit jaar is zo’n tussenliggend jaar. VWS heeft diverse instanties uitgenodigd hun opvattingen over de Nederlandse bloedvoorziening met VWS te delen. In de bijlage staan de instanties genoemd die zijn uitgenodigd2.
Donors
Eerder dit jaar is de wijziging van de Wet inzake bloedvoorziening in verband met risicobeheersing binnen de Bloedvoorzieningsorganisatie in het parlement behandeld. In het debat met de Tweede Kamer heb ik aangegeven dat ik de donors dankbaar ben voor hun belangeloze gift.3 Dankzij deze mensen hebben we in Nederland een eigen bloedvoorziening. De bloedvoorziening is een belangrijk onderdeel in de zorg. Bloedproducten kunnen levensreddend zijn voor bijvoorbeeld slachtoffers van een ernstig verkeersongeluk, vrouwen die veel bloed hebben verloren bij een bevalling, mensen die lijden aan kanker of een bloedziekte, en zo zijn er nog vele andere voorbeelden.
Ik ben blij om te horen dat de wens van oudere donors om langer te mogen doneren dit jaar mogelijk is gemaakt door Sanquin. De maximumleeftijd is namelijk verhoogd van 69 naar 79 jaar.
Donorbestand
In 2017 stonden 331.472 mensen als donor ingeschreven. Dit is iets minder dan 2016, toen stonden 342.600 mensen ingeschreven als donor. De instroom van ingeschreven donors in 2017 was ruim 70.000. Dit aantal is te danken aan 46.119 nieuwe donors en 24.329 donors die al een tijdje niet gedoneerd hadden en opnieuw gevraagd zijn om te doneren. Ondanks de instroom van ruim 70.000 ingeschreven donors is de uitstroom van donors in 2017 hoger geweest, met ruim 80.000, dan de instroom. Dit heeft verschillende oorzaken, waaronder:
– In de afgelopen jaren hebben zich relatief veel jonge vrouwen aangemeld als donor. Zij worden relatief vaker afgekeurd in verband met een te laag ijzergehalte. Het percentage dat terugkomt na afkeuring is relatief laag.
– De trend dat men zich niet meer langdurig ergens aan verbindt (dit is ook zichtbaar bij goede doelen in het algemeen).
– Andere wensen van de donor voor wat betreft de openingstijden. Ik kom hier later op terug.
– Door vaker wijzigende contactgegevens is het voor Sanquin moeilijker om contact met de donor te houden. Als er langere tijd geen contact meer is geweest wordt de donor automatisch uitgeschreven. Sanquin verwacht hier met zijn binnenkort te verschijnen webportal verbetering in.
In zijn donorbestand ziet Sanquin een lichte daling van het aantal volbloeddonors en een groei van plasmadonors. Dit beeld sluit aan bij de ontwikkeling van de behoefte aan bloedproducten. Deze daalt voor kort houdbare bloedproducten en stijgt voor plasmageneesmiddelen. Dit laatste is vooral zichtbaar in de behoefte aan immunoglobulinen4. Voor 2018 heeft Sanquin als doelstelling 65.000 nieuwe donors te werven. Sanquin houdt rekening met een toename van het aantal donors waarbij donatie wordt uitgesteld door de in 2017 ingevoerde ferritine-meting. Met deze meting is er een betere bewaking van de ijzervoorraad bij de donor mogelijk. Sinds de invoering van de meting worden donors met een lage ijzervoorraad, 6 maanden tot 1 jaar uitgesteld van doneren en kunnen zij minder vaak worden opgeroepen. Sanquin heeft op dit moment nog onvoldoende informatie of donors weer terug komen om te doneren na zo’n wachttijd. Sanquin volgt dit zorgvuldig en vult het huidige donorbestand aan met nieuwe donors om eventuele tekorten op te vangen.
Oproep aan donors
De planning van Sanquin om donors op te roepen voor volbloeddonatie is gebaseerd op het aantal beschikbare donors, de bloedgroepverdeling, de afnamelocatie en de voorraad kort houdbare bloedproducten (zoals rode bloedcellen). In de eerste helft van 2018 was het opkomstpercentage lager dan gemiddeld als gevolg van de griepepidemie. Ook het relatief warme weer droeg bij aan een lagere opkomst. Wanneer Sanquin ziet dat de voorraad laag is, worden er uit voorzorg extra acties uitgezet. Zoals een sms of telefonisch contact met de donor met het verzoek gehoor te geven aan de oproepkaart, een extra e-mail naar de donor, berichten op de sociale media, nabellen als de oproeptermijn is verstreken en in juni aandacht in de media.
De aandacht voor bloeddonaties rond de jaarlijkse Wereld Bloeddonordag (14 juni) van de Wereldgezondheidsorganisatie leent zich daar goed voor. In het kader van deze dag heeft Sanquin meegedaan met de internationale Missing Type campagne. Sanquin heeft meerdere bedrijven en organisaties bereid gevonden om de campagne te promoten onder het eigen personeel. Voor anderen was dit zichtbaar doordat Sanquin en de participerende organisaties de bloedgroep aanduidingen A, B, AB en O weglieten uit hun logo of naam. Het doel van Sanquin was in deze campagneperiode 5.000 nieuwe aanmeldingen te genereren. Dit is met ruim 5.200 aanmeldingen behaald.
Sanquin is met al deze acties de maanden juli en augustus goed doorgekomen en eind augustus 2018 was de voorraad weer op orde. Sanquin streeft ernaar om in de komende jaren zijn donorbestand te laten groeien zodat in tijden dat de voorraad daalt Sanquin meer donors kan vragen om te komen doneren.
Donorwerving
In de afgelopen jaren heeft mijn ambtsvoorganger aangegeven dat Sanquin bezig is met het verjongen van het landelijke donorbestand en streeft naar meer diversiteit onder donors.5 De verjonging van de donorpopulatie verloopt gestaag. Sanquin verwacht de komende jaren dat de gemiddelde leeftijd minder hard zal dalen als gevolg van de verhoging van de maximale donorleeftijd van 69 naar 79 jaar. Deze verhoging is in april 2018 ingevoerd. De huidige verjonging van het donorbestand is vooral te danken aan een grote groep jonge vrouwen die zich heeft gemeld. Van de nieuwe aanmeldingen in 2018 is bijna 40% vrouw met een leeftijd tussen de 20 en 35 jaar.
Sanquin streeft naar een voor de bloedvoorziening optimale groep donors, waarbij met name het geslacht, de bloedgroep en de etniciteit van belang zijn. Op dit moment richt Sanquin zijn aandacht op het werven van mannen. Zij mogen vaker doneren en krijgen minder vaak een wachttijd opgelegd vanwege een te laag ijzergehalte. Sanquin probeert nieuwe mannelijke donors te werven door op verschillende manieren verschillende doelgroepen te benaderen. In september 2018 is Sanquin bijvoorbeeld gestart met een nieuwe (online) campagne om meer mannen te werven. In dezelfde periode is tevens, in samenwerking met een gameproducent, een bewustwordingsactie onder gamers georganiseerd. Voor gamers die zich aanmelden als bloeddonor stelt de producent een zogenaamde skin6 ter beschikking.
Sanquin doet onderzoek naar de manier waarop donors met verschillende etniciteit het beste kan worden bereikt met het oog op mogelijke toekomstige werving van bloeddonors uit deze doelgroep. In 2018 heeft Sanquin niet speciaal ingezet op het werven van deze doelgroep omdat er voldoende donors met een bijzonder bloedgroep in het donorbestand aanwezig waren.
Donortevredenheid
In het Ministerieel Plan Bloedvoorziening 2018–2020 is gewezen op de wens van donors om meer in de avonduren te kunnen doneren.7 Verder ervoeren donors lange wachttijden in een afnamelocatie. De wens om meer in de avonduren te doneren is bekend bij Sanquin. Voordat dit gerealiseerd kan worden moet Sanquin de hele route van bloedafname tot aan de aflevering aan het ziekenhuis in ogenschouw nemen. Het langer open blijven van afnamelocaties heeft namelijk gevolgen voor het transport van het bloed en de testbuizen, de laboratoria die de testen moeten uitvoeren, de bewerking van het bloed en het tijdstip waarop alles klaar is zodat het bloed vrijgegeven kan worden. Na donatie van volbloed dient de donatie binnen 24 uur bewerkt te worden. Het langer open blijven van afnamelocaties heeft in de praktijk dus grote gevolgen voor het logistieke proces alsook voor de personele bezetting. Deze gevolgen worden door Sanquin in kaart gebracht. Sanquin pakt per afnamelocatie de wachttijden aan. Op drukke momenten informeert Sanquin donors regelmatig zodat de donor alsnog kan kiezen om op een ander moment te doneren. Op sommige locaties bleek er een te lange wachttijd te zijn voor de keuring voorafgaand aan iedere donatie. In die gevallen heeft Sanquin de keuringscapaciteit uitgebreid.
Een digitale dienstverlening voor de donor zal naar verwachting bijdragen aan kortere wachttijden. Via een beveiligde webportaal zou bijvoorbeeld een digitale vragenlijst al ingevuld kunnen worden. Sanquin werkt nu aan zijn beveiligde Donor Webportaal. Dit portaal is in een vergevorderd stadium. Nog dit jaar moet duidelijk zijn wanneer de eerste donors gebruik kunnen maken van het Donor Webportaal.
Ferritine-meting
In het eerdergenoemde ministerieel plan (Kamerstuk 29 447, nr. 40) is aangegeven dat Sanquin de ferritine-meting (een indicatie voor de ijzervoorraad in het lichaam) gefaseerd invoert. Gedurende het proces worden de ervaring van de donor, de wachttijd van de donor als gevolg van een lage ferritinewaarde en de beschikbaarheid van de donor geanalyseerd. Sanquin vindt bij een relatief groot deel van de donors een lage ferritinewaarde. Ter bescherming van de gezondheid van de donor zal het dan langer duren voordat de donor opnieuw wordt opgeroepen voor donatie en/of kan het aantal donaties per jaar naar beneden worden bijgesteld. In verband met de ferritinemeting verwacht Sanquin dat de komende 5 jaar meer donors nodig zijn om de bloedvoorziening op peil te houden. Geleidelijk zal het opleggen van een wachttijd als gevolg van een lage ferritinewaarde minder voorkomen doordat de donors een donatieplan op maat krijgen, waardoor de ijzervoorraad in het lichaam op peil blijft.
Veiligheid bloedvoorziening
Mannen die seks hebben gehad met andere mannen
Sinds 1 december 2015 kunnen mannen die seks hebben gehad met andere mannen (MSM) bloed doneren 12 maanden na het laatste MSM-contact. Sinds de invoering van de maatregel melden zich gemiddeld 20 MSM per maand aan om donor te worden. Circa tweederde van deze aanmeldingen komt in aanmerking om bloed te doneren, eventueel nadat de wachttijd van 12 maanden na het laatste MSM-contact is verstreken.
Sanquin verzamelt en analyseert gegevens van het huidige donorselectiebeleid rond MSM. Aan de hand van deze gegevens onderzoekt Sanquin of het beleid verder aangepast kan worden. Hierbij worden ook de laatste internationale ontwikkelingen en wetenschappelijke inzichten over infectierisico’s onder MSM betrokken. Sanquin verwacht uiterlijk begin 2019 duidelijkheid te kunnen geven op welke wijze het donorselectiebeleid voor MSM aangepast kan worden zonder dat dit de veiligheid van de bloedvoorziening nadelig beïnvloedt. Daarbij wordt in het bijzonder gedacht aan een wachttijd korter dan 12 maanden na het laatste MSM-contact.
Donorselectiebeleid MSM internationaal
Binnen Europa is de intentie om de wachttijd van 12 maanden na het laatste MSM-contact te verkorten zodra er voldoende waarborgen zijn voor de veiligheid van ontvangers van bloedproducten.
Eind 2017 heeft het Verenigd Koninkrijk (met uitzondering van Noord-Ierland) de wachttijd van 12 maanden voor MSM verkort naar 3 maanden op basis van de aldaar verzamelde epidemiologische gegevens. Er zijn nog geen effecten bekend van deze wijziging. Naar verwachting zal ten minste 2 jaar nodig zijn om zicht te krijgen op de effecten. Op dit moment kan Sanquin de veiligheid van bloedproducten niet garanderen bij een wachttijd van 3 maanden.
De epidemiologie in het Verenigd Koninkrijk is namelijk niet te vergelijken met die van Nederland. In Nederland doen hiv-infecties zich vooral voor onder MSM, terwijl overdracht van hiv-infecties in het Verenigd Koninkrijk zich vooral voordoen tijdens heteroseksuele contacten. Verder is bekend dat een wachttijd van 3 maanden te kort is om hepatitis B-virusinfecties bij donors in alle gevallen met laboratoriumtesten te vinden en overdracht van het virus via bloedproducten te voorkomen. In Nederland hebben MSM een verhoogde kans op het hepatitis B-virus. Ook om die reden is het nodig om terughoudend te zijn bij het direct toelaten van MSM als bloeddonor. Belangrijk hierbij is een wachttijd na het laatste MSM-contact in acht te nemen, die volstaat om overdracht van een virus zoals het hepatitis B-virus via bloedproducten te voorkomen.
Denemarken heeft aangekondigd zijn donorselectiebeleid rond MSM in 2019 te wijzigen naar een wachttijd van 4 maanden na het laatste MSM-contact en mogelijk worden MSM toegelaten die een monogame relatie hebben. Nadere details over de beleidswijziging in Denemarken, waaronder een risicoanalyse en hoe de veiligheid van de bloedvoorziening gegarandeerd gaat worden, zijn nog niet bekend.
Naar verwachting komt de Raad van Europa in 2019 met aanbevelingen over (seksueel) risicogedrag van bloeddonors en hoe de Europese lidstaten hier mee om kan gaan met het oog op de veiligheid voor de ontvangers van bloedproducten. In de aanbevelingen zal naar verwachting specifieke aandacht zijn voor bloeddonatie door MSM en de daarbij in acht te nemen voorwaarden. 2019 is later dan verwacht doordat de afgelopen jaren weinig nieuwe wetenschappelijke gegevens beschikbaar zijn gekomen. Ook zijn er weinig ervaringscijfers beschikbaar uit Westerse landen die de permanente uitsluiting van MSM hebben vervangen door een tijdelijk uitstelbeleid na het laatste MSM-contact.
Hepatitis E-virus en bloeddonaties
Mijn ambtsvoorganger had voorlopig ingestemd met het testen van bloeddonaties op hepatitis E-virus (HEV).8 Sanquin is in juli 2017 gestart met het testen op HEV. Omdat er nog veel onbekend was over HEV is indertijd de Gezondheidsraad om advies verzocht over het nut en de noodzaak van deze maatregel. De Gezondheidsraad heeft eind juli zijn advies gepubliceerd en aan uw Kamer aangeboden.9 Mijn reactie op dit advies volgt hieronder.
In zijn advies «Testen van bloeddonaties op hepatitis E-virus» adviseert de Gezondheidsraad voorlopig door te gaan met het testen. Bloeddonoren zijn namelijk regelmatig besmet met HEV en mensen die bloedproducten ontvangen hebben vaak een verzwakt afweersysteem waardoor besmetting voor deze patiënten ernstige gevolgen kan hebben.
Daarnaast adviseert de raad een afwegingskader voor kosteneffectiviteit in de bloedvoorziening te ontwikkelen. Met zo’n kader kunnen de kosten dan op een consequente manier meegewogen worden in een toekomstige besluitvorming. Besmette varkens zijn in Nederland de belangrijkste bron van HEV en overdracht vindt plaats via besmette voedselproducten. De raad adviseert daarom eveneens te onderzoeken welke maatregelen in de varkenssector en de voedselketen getroffen kunnen worden. Tot slot adviseert de raad het belang van het testen van bloeddonaties op HEV over enkele jaren opnieuw te beoordelen. Er zal dan meer onderzoek gedaan zijn naar besmettingen onder bloeddonors, de kans op overdracht bij lage hoeveelheden virusdeeltjes en de ziektelast en behandelbaarheid van HEV bij patiënten.
Ik kan mij vinden in de adviezen van de Gezondheidsraad. Het testen van de bloeddonaties zal voorlopig voortgezet worden. Ik zal bezien hoe het ontwikkelen van een afwegingskader en het te zijner tijd opnieuw beoordelen van het belang van het testen op HEV opgenomen kan worden in het werkprogramma van de Gezondheidsraad. Wat betreft het onderzoeken welke maatregelen in de varkenssector en de voedselketen getroffen kunnen worden, kan ik u het volgende melden. In de afgelopen jaren is het Deskundigenberaad hepatitis E diverse malen bijeen gekomen. In dit beraad komen medisch specialisten en deskundigen van diverse instellingen en organisaties bijeen die betrokken zijn bij de infectiebestrijding. De adviezen van het Deskundigenberaad hepatitis E op het terrein van de varkenshouderij en voedsel zijn grotendeels opgevolgd.
Zo zijn de testen voor dieren, voedsel en mensen verbeterd en op elkaar afgestemd. Voor patiënten die behoren tot de risicogroepen10 is een voedingsadvies opgesteld. Dit advies is verspreid onder de betrokken zorgverleners en openbaar gemaakt op de websites van het Voedingscentrum en het RIVM11. Door het patiëntencontrole- onderzoek HEVIG en onderzoek van de NWVA12 is inmiddels ook bekend dat HEV niet alleen in paté en leverworst zit. In Nederland wordt HEV voornamelijk opgelopen door consumptie van droge gefermenteerde worsten van rauw varkensvlees zoals cervelaat, salami, en boerenmetworst.
Het voedingsadvies is hierop aangepast en de vleeswarenindustrie past inmiddels maatregelen toe om te voorkomen dat er lever in rauwe worst terecht komt. Naar aanleiding van een advies van het European Food Safety Authority13 wordt in Europees verband gekeken naar mogelijke nadere maatregelen. Verder start het RIVM dit jaar met een onderzoek naar mogelijke veranderingen in de epidemiologie en de actuele prevalentie van HEV in de Nederlandse varkensstapel. Deze ontwikkelingen zijn in lijn met de aanbeveling van de Gezondheidsraad.
Bloedproducten
Behoefte bloedproducten
Mijn ambtsvoorganger heeft in de afgelopen jaren al vaker aangegeven dat het gebruik van rode bloedcellen al jaren daalt. Ik verwijs u naar de Actualiteitenbrief bloedvoorziening 2015 voor de factoren die hebben bijgedragen aan deze daling.14 De trend van de laatste jaren laat een daling zien van ongeveer 2%. De verwachting is dat als gevolg van een toename van evidence based onderzoek naar optimaal gebruik van bloedproducten bij hemato-oncologische patiënten15 de behoefte aan rode bloedcellen nog verder zal dalen.
Iedereen heeft er baat bij wanneer er sprake is van een zinnig en zuinig gebruik van bloedproducten. We moeten enerzijds zuinig zijn met de belangeloze giften van donors en anderzijds is nulrisico bij dit soort producten alleen mogelijk door ze niet te gebruiken. Het gevolg van een verdere daling in het gebruik van kort houdbare bloedproducten is dat Sanquin de vaste lasten over steeds minder producten kan verdelen. Dit zou in de toekomst mogelijk tot hogere (kost)prijzen leiden. Sanquin mag op grond van artikel 14 van de Wet inzake bloedvoorziening geen hogere prijs voor zijn kort houdbare bloedproducten vragen dan de kostprijs. Ik vind het belangrijk dat Sanquin inzicht geeft aan zijn afnemers hoe de prijzen van de bloedproducten zijn opgebouwd. Ik heb Sanquin daarom verzocht dit inzicht te bieden, naast de huidige vermelding ervan op zijn website.
Plasmageneesmiddelen
In het Ministerieel Plan Bloedvoorziening 2018–2020 is u gemeld hoe Sanquin Plasma Products BV (SPP) zich inzet om zijn productieproces te wijzigen.16
De aanpassing van zijn productieproces ligt in 2018 op schema. SPP dient eind september 2018 de eerste set gegevens in van het nieuwe productieproces bij het College ter Beoordeling van Geneesmiddelen (CBG). Als er voldoende gegevens beschikbaar zijn om tot een oordeel te komen kan SPP na goedkeuring van het CBG starten met het invoeren van zijn nieuwe productieproces. Tot het zover is zorgt SPP nog steeds voor vervanging door gelijkwaardige alternatieven. Wanneer dit niet mogelijk is gelden risicobeperkende maatregelen, die zijn opgelegd door het CBG, zoals het intensief volgen van de mogelijke risico’s van de producten. De vervangende producten zijn in overleg met de Inspectie Gezondheidszorg en Jeugd en het CBG ingezet en worden zonder meerkosten beschikbaar gesteld aan Nederlandse ziekenhuizen en patiënten.
Plasma als grondstof voor plasmageneesmiddelen
Op grond van de Wet inzake bloedvoorziening mag alleen Sanquin bloed en plasma inzamelen in Nederland. Behalve als bloedproduct dient het ingezamelde plasma eveneens als grondstof voor de productie van plasmageneesmiddelen (zoals stollingsfactoren en immunoglobulinen). De stichting Sanquin levert de plasma aan haar dochteronderneming Sanquin Plasma Products BV. De prijs voor het leveren van het door de stichting Sanquin ingezamelde plasma wordt door de Minister voor Medische Zorg vastgesteld. In de Actualiteitenbrief Bloedvoorziening 2016 is aangegeven dat deze prijs gebaseerd is op de Europese markt.17Mijn ambtsvoorganger heeft de afgelopen jaren de jaarlijks vastgestelde prijs geïndexeerd voor lonen en prijzen. Voor het komende jaar continueer ik deze werkwijze.
De prijs van het plasma als grondstof wordt geïndexeerd ten opzichte van 2018 met de ontwikkeling van lonen en prijzen en kapitaallasten. De verwachte gewogen gemiddelde prijsindex voor het jaar 2019 is 3,42%. Daarmee komt de prijs voor volbloedplasma naar verwachting uit op circa € 97 en voor afereseplasma op circa € 114 per kilogram. De definitieve bedragen volgen uit de begroting van de stichting Sanquin voor het jaar 2019.
Inzameling
In het eerdergenoemde ministerieel plan (Kamerstuk 29 447, nr. 40) werd aangegeven dat Sanquin onderzoekt hoe de inzameling van plasma doelmatiger en efficiënter kan. De behoefte aan plasma als grondstof stijgt namelijk jaarlijks door de (wereldwijde) toenemende behoefte aan immunoglobulinen. Sanquin treft voorbereidingen om een plasma only inzamelingscentrum neer te zetten. De schaalgrootte, automatisering van processen en efficiënte logistiek moeten voor een doelmatiger donatieproces van plasma zorgen. Sanquin zal daarbij een aparte wervingscampagne voor plasmadonors opzetten. Het uitgangspunt hierbij is dat dit geen nadelige effecten heeft op de donorbereidheid en de doelmatigheid van de bloedvoorziening.
Wereldwijd is sprake van een tekort aan plasma als grondstof voor met name de productie van immunoglobulinen. In de European Blood Alliance18 is aandacht voor het (doelmatiger) inzamelen van plasma in Europa en het tegen gaan van verlies van volbloedplasma. Ook een werkgroep binnen de Raad van Europa buigt zich over de beschikbaarheid van plasma als grondstof.
Structuurwijziging Sanquin
De stichting Sanquin heeft in de afgelopen jaren meerdere dochterondernemingen opgericht. In deze BV’s is het merendeel van de niet-wettelijke activiteiten van de stichting ondergebracht. Onder niet-wettelijke activiteiten worden alle activiteiten verstaan die niet volgen uit de Wet inzake bloedvoorziening. Uw Kamer is hierover regelmatig geïnformeerd door middel van onder andere de jaarlijkse actualiteitenbrief en het driejaarlijkse ministerieel plan.19
In 2015 is de productie van plasmageneesmiddelen uit Nederlands plasma en in opdracht van derden (met plasma uit het buitenland) ondergebracht in de dochteronderneming Sanquin Plasma Products BV (SPP). Daarmee zijn ook de werkzaamheden voor de uitvoering van de wettelijke taak rond plasmageneesmiddelen, het beschikbaar stellen van deze geneesmiddelen uit Nederlands plasma, uitbesteed aan SPP. Tot de inwerkingtreding van de wetswijziging20 is de uitvoering van deze wettelijke taak in een juridisch bindend convenant tussen het Ministerie van VWS, de stichting Sanquin en SPP gewaarborgd.
Begin 2017 zijn andere niet-wettelijke activiteiten van de stichting in de dochterondernemingen Sanquin Reagents BV en Sanquin Diagnostiek BV ondergebracht. Reagents BV ontwikkelt een breed pakket aan testproducten (zogenaamde reagentia) waarmee bloedgroepen en immunologische eigenschappen of afwijkingen in bloedmonsters aangetoond kunnen worden.
Deze testproducten worden bijvoorbeeld in het belang van de patiëntdiagnostiek gebruikt. Diagnostiek BV levert advies en diagnostische diensten op het gebied van bloedtransfusie en immunologie voor ziekenhuizen, verloskundige praktijken en farmaceutische bedrijven. Als bijvoorbeeld een patiënt binnen een ziekenhuis moeilijk te diagnosticeren is voor het matchen van een bloedproduct, dan wordt de vraag voorgelegd aan Diagnostiek BV. Het gaat hier vaak om complexe diagnostiek. De transfusielaboratoria binnen ziekenhuizen hebben in een aantal gevallen niet de expertise, ervaring en/of benodigde testproducten in huis om zo’n bijzonder complexe diagnostiek uit te kunnen voeren. Verder wordt regelmatig een beroep gedaan op de expertise van Diagnostiek BV om het kennisniveau van de medewerkers van het transfusielaboratorium actueel te houden. Deze bij- en nascholingen dragen bij aan een hoog kennisniveau in Nederland op het gebied van de transfusiegeneeskunde.
In het najaar van 2017 is Sanquinnovate BV opgericht. Voor de stichting Sanquin is dit een broedplaats voor ideeën voor nieuwe producten en diensten, op geleide van de medische behoeften. Nieuwe ideeën kunnen in deze BV divisie-overstijgend opgepakt worden en als business case verder worden ontwikkeld. Waar nodig met externe partners.
Andere niet-wettelijke activiteiten in de stichting Sanquin bevinden zich in de divisie Research & LabServices en het onderdeel Tissues & Cells. Dit onderdeel bestond uit de navelstrengbloedbank, de botbank en het stamcellaboratorium. In 2017 is de botbank samengegaan met de weefselinstelling BISLIFE (nu ETB-BISLIFE) en afgelopen zomer is het stamcellaboratorium overgegaan naar het UMC Groningen. Een deel van de Concernstaf en diensten zet zich in voor de dochterondernemingen en dit deel kan als een niet-wettelijke activiteit worden beschouwd.
Onlangs is het Besluit niet-wettelijke activiteiten Bloedvoorzieningsorganisatie gepubliceerd.21 Hierin worden grenzen gesteld aan de niet-wettelijke activiteiten binnen de stichting. Het Besluit moet nog in werking treden. Ik kom hier later op terug.
Organogram Sanquin groep anno 2018
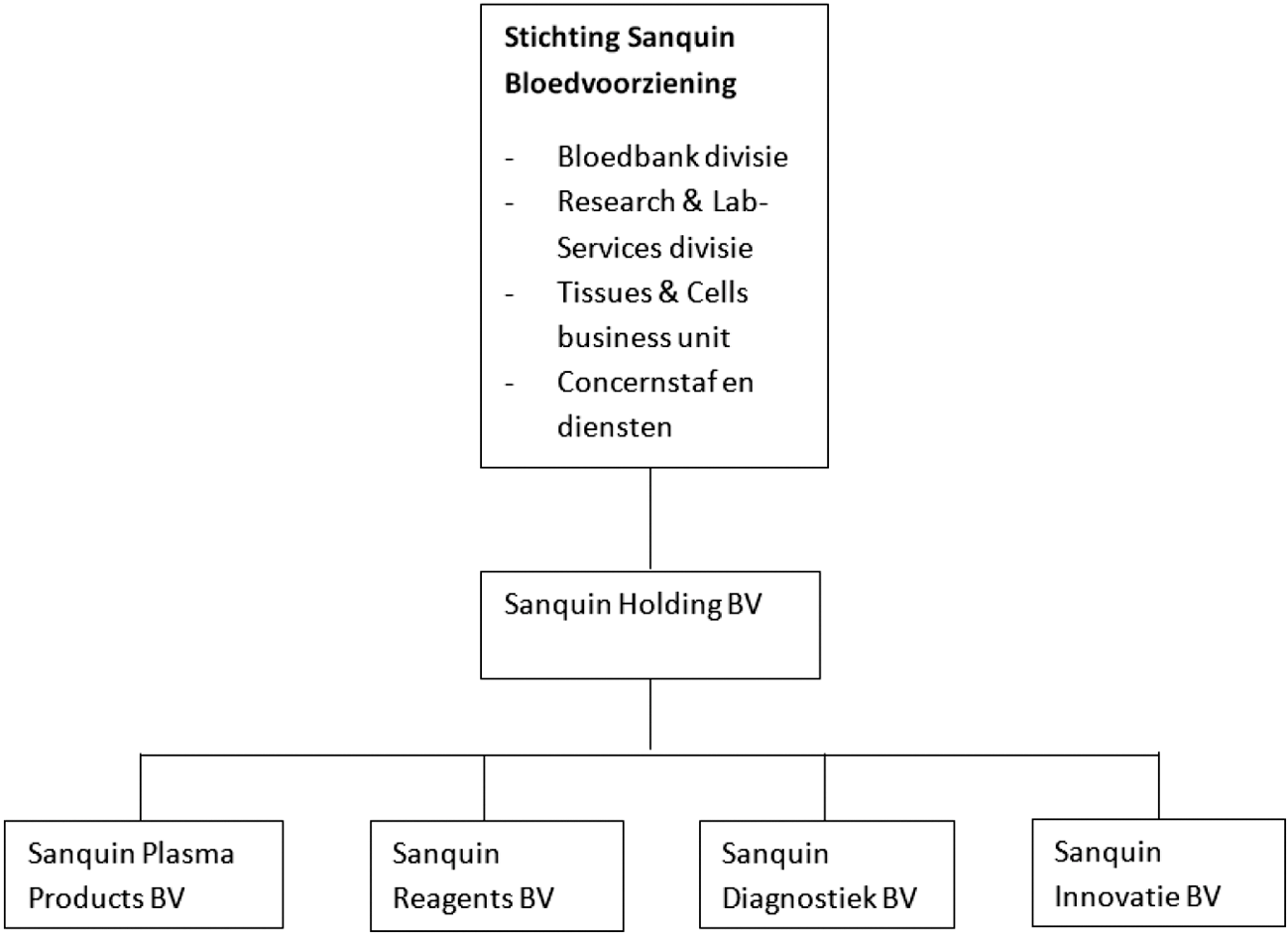
Ontwikkelingen SPP
In mei van dit jaar heb ik de Tweede Kamer geïnformeerd over de ontwikkelingen bij de dochteronderneming Sanquin Plasma Products BV (SPP).22 Door ontwikkelingen op de internationale markt is een strategische heroriëntatie van SPP actueel. Ik had al aangegeven dat de continuïteit van de bloedvoorziening en de beschikbaarheid van plasmageneesmiddelen in Nederland, voor mij voorop staan. Daarom vind ik het belangrijk dat SPP in zijn oriëntatie in ieder geval rekening houdt met de volgende randvoorwaarden:
– De Bloedvoorzieningsorganisatie blijft eindverantwoordelijk voor de wettelijke taken op grond van artikel 3, eerste lid, Wet inzake bloedvoorziening.
– De uitkomst van de strategische heroriëntatie heeft geen negatieve gevolgen voor de Nederlandse donatiebereidheid.
– Het deel aan plasmageneesmiddelen die (mede) bereid zijn uit Nederlands plasma wordt in eerste instantie aan de Nederlandse markt aangeboden.
– Het behoud van een productiefaciliteit voor plasmageneesmiddelen in Nederland.
In mijn genoemde brief aan de Tweede Kamer heb ik de brief van Sanquin over de strategische heroriëntatie bijgesloten (bijlage bij Kamerstuk 29 447, nr. 42). Sanquin gaf aan dat er meerdere bedrijven zijn die belangstelling hebben geuit voor een bepaalde vorm van een strategische partnerschap met SPP. Deze gesprekken zijn nog steeds gaande.
Wijziging Wet inzake bloedvoorziening
Naar verwachting zal de Wet van 18 april 2018 tot wijziging van de Wet inzake bloedvoorziening in verband met risicobeheersing binnen de Bloedvoorzieningsorganisatie23 per 1 januari 2019 in werking treden. Ik ga in deze brief kort in op de belangrijkste wijzigingen. Tevens schets ik de stand van zaken van de voorbereidingen.
De wijzigingswet geeft een grondslag om bij algemene maatregel van bestuur een maximum te stellen aan de niet-wettelijke activiteiten van de Bloedvoorzieningsorganisatie. Inmiddels is het Besluit niet-wettelijke activiteiten Bloedvoorzieningsorganisatie gepubliceerd.24 Het besluit omvat het volgende:
de totale kosten van de niet-wettelijke activiteiten binnen de stichting Sanquin mogen niet meer dan tien procent zijn van de totale kosten van de stichting.Voor de staf- en concerndiensten die de stichting voor haar dochterondernemingen uitvoert geldt een andere grens. Deze kosten voor de dochterondernemingen mogen niet meer zijn dan de totale kosten van staf- en concerndiensten die voor de stichting worden gemaakt. Een andere grens voor de staf- en concerndiensten ten behoeve van dochterondernemingen is gerechtvaardigd omdat de uitvoering van de wettelijke taken door de stichting profiteert van schaalvoordelen doordat deze activiteiten gezamenlijk worden uitgevoerd.
Met de wetswijziging wordt het ook mogelijk dat de Bloedvoorzieningsorganisatie, na instemming van de Minister voor Medische Zorg, de werkzaamheden van bepaalde wettelijke taken uit kan laten voeren door andere rechtspersonen. De procedure voor het verkrijgen van een toestemming zal vastgelegd worden in een beleidsregel. De Bloedvoorzieningsorganisatie blijft verantwoordelijk voor het geheel van de bloedvoorziening. De beleidsregel is in voorbereiding en zal dit najaar gereed zijn. De beleidsregel zal in de Staatscourant worden gepubliceerd. Daarnaast kan de Minister de procedure voor het vaststellen van de prijs van plasma als grondstof voor plasmageneesmiddelen vastleggen in een ministeriële regeling. Ik zal in 2019 beslissen of ik gebruik maak van deze mogelijkheid.
De motie van het lid Van de Berg verzoekt de regering de Tweede Kamer jaarlijks te informeren over alle relevante zaken rond de financiële situatie van de stichting Sanquin en de dochterondernemingen van de stichting.25 Op basis van de nieuwe juridische structuur en als gevolg van de wijziging van de wet zal Sanquin zorg dragen voor aparte jaarrekeningen van de stichting en de dochterondernemingen. De verwachting is dat de wijziging met ingang van 1 januari 2019 in werking treedt. Dit betekent dat ik rond medio 2019 uitvoering kan geven aan deze motie.
Navelstrengbloedbank
In 2013 heeft mijn ambtsvoorganger onder voorwaarden ingestemd dat Sanquin € 8 miljoen van het eigen vermogen van de divisie Bloedbank gebruikt voor de uitbreiding en verbetering van de navelstrengbloedbank. Het is eerder gebleken dat de navelstrengbloedbank minder snel groeit dan aanvankelijk verwacht.26
Hierdoor kan de navelstrengbloedbank niet aan de gestelde voorwaarde van kostenneutraliteit voldoen.
De afgelopen periode heb ik laten onderzoeken of de noodzaak nog bestaat voor het behoud van een navelstrengbloedbank in Nederland. Ook is onderzocht of dit een bekostiging uit de financiële middelen van de Bloedbank divisie (of anderszins) rechtvaardigt. De onderzoekers hebben ook gekeken naar het relevante juridische kader en alternatieve organisatievormen. Daarbij zijn diverse scenario’s de revue gepasseerd waaronder voortzetting van de huidige situatie al of niet in afgeslankte vorm of een gehele beëindiging van de activiteiten van de navelstrengbloedbank. Ik verwacht binnenkort het onderzoeksrapport.
Na afronding van het onderzoeksrapport zal ik de Tweede Kamer uitgebreider informeren over de resultaten van dit onderzoek. Mede op basis van dit rapport zal ik beslissen over de toekomst van de navelstrengbloedbank in Nederland.
Stamceltransplantaties worden toegepast bij de behandeling van ernstig zieke patiënten zoals leukemiepatiënten. Het gaat om transplantaties met zogenaamde hematopoietische stamcellen, onder andere verkregen uit navelstrengbloed. Ik vind het belangrijk om te constateren dat ook zonder de navelstrengbloedbank nog steeds stamcellen beschikbaar zijn voor stamceltransplantaties. Deze stamcellen zijn uit andere bronnen dan navelstrengbloed afkomstig of verkregen via andere instellingen op de internationale markt.
De Minister voor Medische Zorg, B.J. Bruins
Testen van bloeddonaties op hepatitis E-virus, Gezondheidsraad (nr. 2018/18), 31 juli 2018. Zie ook: https://www.gezondheidsraad.nl/nl/taak-werkwijze/werkterrein/preventie/testen-van-bloeddonaties-op-hepatitis-e-virus.
Dit zijn eiwitten afkomstig uit plasma die onder meer toegepast worden bij patiënten met een aangeboren afweerstoornis, bij patiënten met leukemie of beenmergkanker met terugkerende bacteriële infecties en patiënten na een stamceltransplantatie.
Patiënten met een zwak afweersysteem, zoals transplantatiepatiënten en patiënten met leukemie.
Public health risks associated with hepatitis E virus (HEV) as a food-borne pathogen, EFSA journal 2017; 15(7): 488, zie ook: http://www.efsa.europa.eu/en/efsajournal/pub/4886.
Dit zijn patiënten met kwaadaardige ziekten van bloed, beenmerg en/of lymfeklieren (voorbeelden: leukemie, ziekte van Hodgkin en ziekte van Kahler). Deze patiënten gebruiken relatief veel rode bloedcellen.
Wijziging van de Wet inzake bloedvoorziening in verband met risicobeheersing binnen de Bloedvoorzieningsorganisatie (Stb. 2018, nr. 136).
Kopieer de link naar uw clipboard
https://zoek.officielebekendmakingen.nl/kst-29447-44.html
De hier aangeboden pdf-bestanden van het Staatsblad, Staatscourant, Tractatenblad, provinciaal blad, gemeenteblad, waterschapsblad en blad gemeenschappelijke regeling vormen de formele bekendmakingen in de zin van de Bekendmakingswet en de Rijkswet goedkeuring en bekendmaking verdragen voor zover ze na 1 juli 2009 zijn uitgegeven. Voor pdf-publicaties van vóór deze datum geldt dat alleen de in papieren vorm uitgegeven bladen formele status hebben; de hier aangeboden elektronische versies daarvan worden bij wijze van service aangeboden.
